AA
Alma A
15 Desember 2021 06:22
Iklan
AA
Alma A
15 Desember 2021 06:22
Pertanyaan
dalam reaksi kesetimbangan: N2(g) + 3H2(g) <-> 2NH3(g) jika pada kesetimbangan terdapat 1 mol N2r 2 mol H2r dan 1 mol NH3 serta tekanan total gas adalah 10 atm maka harga Kp reaksi tersebut adalah.... A. 1/2 B. 1/5 C. 1/9 D. 1/20 E. 1/50
3
2
Iklan
DA
D. Aprilia
Mahasiswa/Alumni Universitas Pendidikan Indonesia
13 Januari 2022 16:20
Jawaban terverifikasi
Halo Alma :) Jadi, jawaban yang tepat adalah E. Yuk simak pembahasannya berikut ini! Reaksi kesetimbangan adalah reaksi reversible (dapat balik), artinya produk dapat bereaksi kembali membentuk reaktan. Reaksi kesetimbangan ditandai dengan lambang “⇌“ . Saat reaksi mencapai keadaan setimbang, kita dapat menentukan tetapan kesetimbangan (K). Berdasarkan tekanannya, tetapan kesetimbangan dilambangkan dengan Kp. Untuk reaksi : aA + bB ⇌ cC + dD maka rumus Kp nya (perhatikan gambar ke-1) : Diketahui pada soal : mol saat setimbang dari N2 = 1 mol, H2 = 2 mol, NH3 = 1 mol, maka mol total saat setimbang nya = 1 + 2 + 1 = 4 mol P total = 10 atm Sebelum menentukan Kp, kita hitung dulu tekanan parsial masing-masing zat. (perhatikan perhitungannya pada gambar ke-2) Dengan reaksi : N2 + 3H2 ⇌ 2NH3 , maka perhitungan Kp nya (perhatikan gambar ke-3)


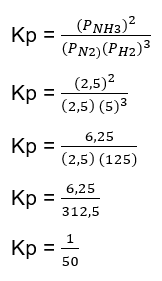
· 0.0 (0)
Iklan
HH
Hendri H
19 Mei 2023 12:18
Dari reaksi kesetimbangan dibawah ini yang akan bergeser ke kanan jika tekanan di perbesar adalah …..
· 0.0 (0)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



