IF
Ichsanul F
10 Mei 2022 06:45
Iklan
IF
Ichsanul F
10 Mei 2022 06:45
Pertanyaan
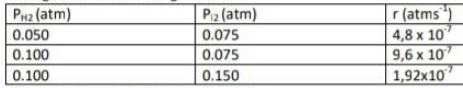
Dalam fasa gas, hidrogen dan iodin dapat bereaksi menghasilkan HI. Analisis laju awal reaksi terhadap tekanan parsial gas hidrogen dan iodin pada suhu tertentu menghasilkan data sebagai berikut. Orde total dari reaksi tersebut adalah .... A. 1 B. 2 C. 3 D. 4 E. 5
11
2
Iklan
AA
A. Atikasari
Mahasiswa/Alumni Universitas Negeri Yogyakarta
10 Mei 2022 22:53
Jawaban terverifikasi
Jawaban yang benar adalah opsi B. Laju reaksi adalah perubahan konsentrasi tiap satuan waktu, perubahan konsentrasi dapat berupa berkurangnya konsentrasi reaktan atau bertambahnya konsentrasi produk tiap satuan waktu. Persamaan laju reaksi dapat dituliskan sebagai berikut: v = k [A]^m[B]^n Dimana, v= Laju reaksi (mol L⁻¹ s⁻¹); k= konstanta laju reaksi; n= orde reaksi zat B; m= orde reaksi zat A. • Apabila laju dinyatakan dengan r (atm/s), maka rumus laju adalah: r = (PA)^m (PB)^n Dimana merupakan tekanan parsial gas, r adalah laju yang dinyatakan dalam atm/s. Untuk mencari orde reaksi m dan n, dapat menggunakan perhitungan berikut: >> Percobaan 1 dan Percobaan 2 saat konsentrasi H₂ berubah sedangkan konsentrasi I₂ tidak berubah. r₂ : r₁ = ((P H₂)₂ : (P H₂)₁)^m x ((P I₂)₂ : (P I₂)₁)^n 9,6 x 10⁻⁷ atm/s : 4,8 x 10⁻⁷ atm/s = (0,100 atm : 0,050 M)^m x (0,075 atm : 0,075 atm)^n 2 = 2^m x 1^n 2 = 2^m x 1 2 = 2^m m = 1 >> Percobaan 2 dan Percobaan 3 saat konsentrasi H₂ tidak berubah sedangkan konsentrasi I₂ berubah, untuk r₃ seharusnya 1,92 x 10⁻⁶ ya^^ r₃ : r₂ = ((P H₂)₃ : (P H₂)₂)^m x ((P I₂)₃ : (P I₂)₂)^n 1,92 x 10⁻⁶ atm/s : 9,6 x 10⁻⁷ atm/s = (0,100 atm : 0,100 atm)^m x (0,150 atm : 0,075 atm)^n 2 = 1^m x 2^n 2 = 1 x 2^n 2 = 2^n n = 1 Berdasarkan perhitungan di atas, maka: • Orde reaksi H₂ = m = 1 • Orde reaksi I₂ = n = 1 • Orde reaksi total = m + n = 1 + 1 = 2 Jadi, orde total dari reaksi pada soal adalah 2.
· 0.0 (0)
Iklan
GC
Galuh C
08 Maret 2023 12:31
- Dalam fasa gas, hidrogen dan iodin dapat bereaksi menghasilkan HI. Analisis laju awal reaksi terhadap tekanan parsial gas hidrogen dan lodin pada suhu tertentu r(atm * s ^ - 1) 4.8 * 10 ^ - 7 9, 6 * 10 ^ - 7 1.92 * 10 ^ - 7 0.150 0.075 0.075 P_{12} atm) menghasilkan data sebagai berikut 0.100 0.100 0.050 PHz (atm)
· 0.0 (0)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



