AH
Ai H
28 Juli 2022 13:53
Iklan
AH
Ai H
28 Juli 2022 13:53
Pertanyaan
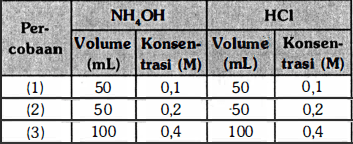
Campuran larutan NH4OH dengan larutan HCl dapat menghasilkan garam yang terhidrolisis sebagian. Dari percobaan diperoleh data seperti terdapat dalam tabel berikut. Jika diketahui Kb NH4OH = 1,0 x 10^-5 maka urutan kenaikan pH campuran adalah ... A. (1), (2), dan (3) B. (1), (3), dan (2) C. (2), (1), dan (3) D. (2), (3), dan (1) E. (3), (2), dan (1)
8
1
Iklan
YY
Y. Yosua
22 Agustus 2022 02:42
Jawaban terverifikasi
Jawaban : E. (3), (2), dan (1) Garam asam adalah garam yang dihasilkan dari reaksi asam kuat dan basa lemah yang habis bereaksi. NH4OH dan HCl bereaksi menurut persamaan berikut: NH4OH + HCl -> NH4Cl + H2O Dengan perbandingan mol dan koefisien, diperoleh: mol NH4OH/mol HCl = koefisien NH4OH/koefisien HCl mol NH4OH/mol HCl = 1/1 mol NH4OH = mol HCl Dengan perbandingan mol dan koefisien, juga diperoleh: mol NH4OH/mol NH4Cl = koefisien NH4OH/koefisien NH4Cl mol NH4OH/mol NH4Cl = 1/1 mol NH4OH = mol NH4Cl Agar kedua zat habis bereaksi, maka NH4OH dan HCl harus direaksikan dengan mol yang sama. Pada percobaan (1), (2), dan (3), NH4OH dan HCl telah direaksian dengan volume dan konsentrasi yang sama sehingga molnya sama dan membentuk garam asam. NH4Cl apabila terlarut dalam air membentuk reaksi berikut : NH4Cl-> NH4^+ + Cl^- Sehingga diperoleh [NH4Cl] = [NH4^+]. Asumsikan Kb = 10^-5, maka dapat diperoleh [H^+] sebagai berikut : [H^+] = √Kw/Kb.[NH4^+] [H^+] = √Kw/Kb.[NH4Cl] [H^+] berbanding lurus dengan [NH4Cl]. Semakin tinggi pH, semakin rendah [H^+] begitupun sebaliknya. Oleh karena itu, semakin tinggi pH, semakin rendah juga [NH4Cl] begitupun sebaliknya. Percobaan 1 : [NH4Cl] = mol NH4Cl/Vakhir [NH4Cl] = mol NH4OH/(V NH4OH + V HCl) [NH4Cl] = [NH4OH].V HCl/(V NH4OH + V HCl) [NH4Cl] = 0,1 M.50 mL/(50 mL + 50 mL) [NH4Cl] = 5 mmol/100 mL [NH4Cl] = 0,05 M Percobaan 2 : [NH4Cl] = mol NH4Cl/Vakhir [NH4Cl] = mol NH4OH/(V NH4OH + V HCl) [NH4Cl] = [NH4OH].V HCl/(V NH4OH + V HCl) [NH4Cl] = 0,2 M.50 mL/(50 mL + 50 mL) [NH4Cl] = 10 mmol/100 mL [NH4Cl] = 0,1 M Percobaan 3 : Percobaan 1 : [NH4Cl] = mol NH4Cl/Vakhir [NH4Cl] = mol NH4OH/(V NH4OH + V HCl) [NH4Cl] = [NH4OH].V HCl/(V NH4OH + V HCl) [NH4Cl] = 0,4 M.100 mL/(100 mL + 100 mL) [NH4Cl] = 40 mmol/200 mL [NH4Cl] = 0,2 M Dengan demikian, urutan kenaikan pH campuran adalah E. (3), (2), dan (1).
· 3.0 (1)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



