NA
Nurul A
04 Maret 2022 02:06
Iklan
NA
Nurul A
04 Maret 2022 02:06
Pertanyaan
Buat grafik kecenderungan energi ionisasi dan afinitas elektron unsur-unsur gas mulia terhadap jari-jari atom dari kecil ke besar. Sifat kecenderungannya adalah ............... .
3
2
Iklan
DA
D. Aprilia
Mahasiswa/Alumni Universitas Pendidikan Indonesia
11 Maret 2022 10:43
Jawaban terverifikasi
Halo Nurul :) Jadi, grafik energi ionisasi terhadap jari-jari atom cenderung menurun, sedangkan grafik afinitas terhadap jari-jari atom cenderung meningkat. Perhatikan grafiknya pada gambar yaaa. Unsur pada golongan VIIIA disebut unsur gas mulia karena unsur ini sangat stabil (sukar bereaksi). Kestabilan ini karena konfigurasi elektron unsur gas mulia memenuhi aturan oktet (dan duplet untuk Helium). Unsur gas mulia terdapat sebagai molekul monoatomik. Kestabilannya juga dicerminkan dari energi ionisasinya yang sangat besar sedangkan afinitas nya sangat rendah. Dari tabel 3.4 diatas diketahui bahwa jari-jari atom dari atas ke bawah (He ke Rn) semakin besar. Begitu pula dengan afinitas elektronnya. Berikut data afinitas elektron unsur gas mulia dalam satuan kJ/mol : He = 21 Ne = 29 Ar = 35 Kr = 39 Xe = 41 Rn = 41 sehingga apabila kita gambarkan grafik afinitas terhadap jari-jari atom dari kecil ke besar, akan didapat grafik yang cenderung meningkat. Sedangkan untuk energi ionisasi semakin bawah semakin kecil, sehingga grafiknya terhadap jari-jari atom akan menurun.
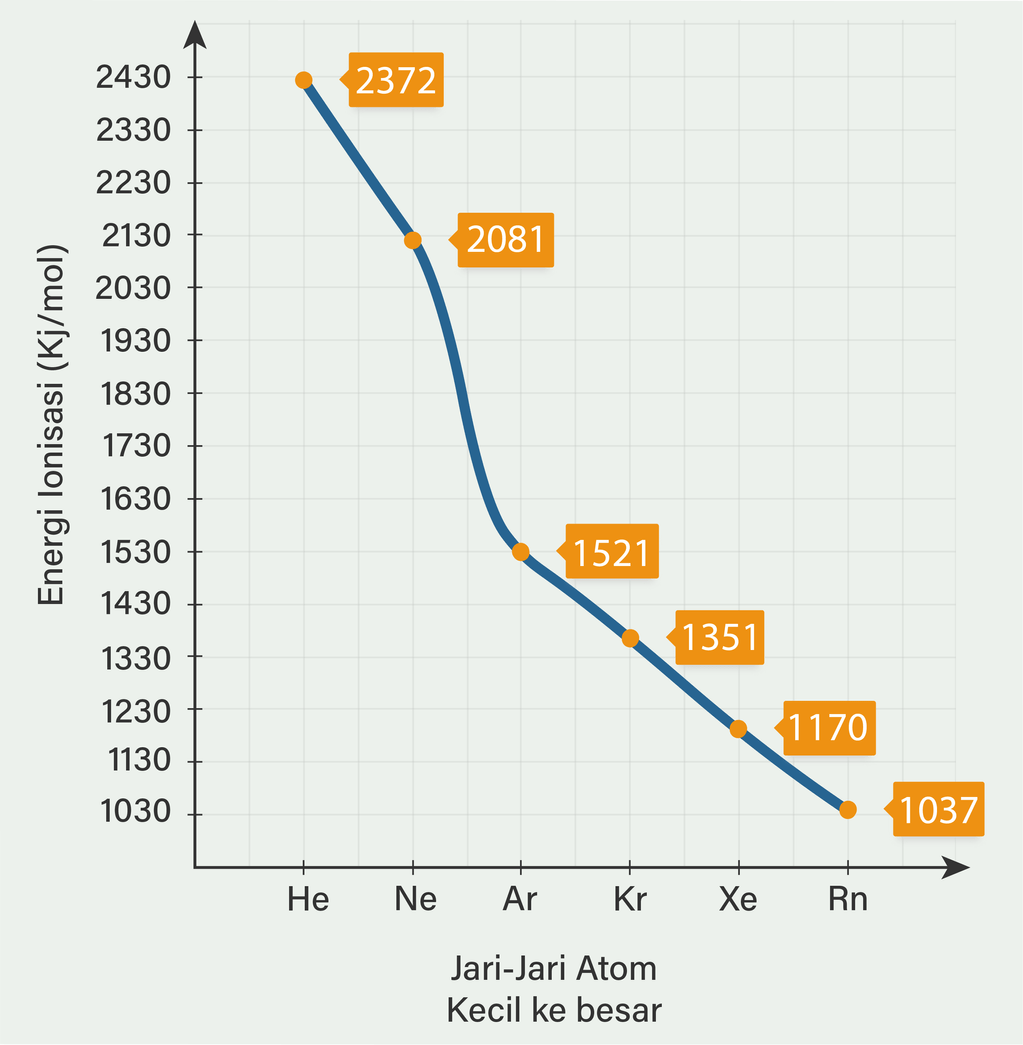
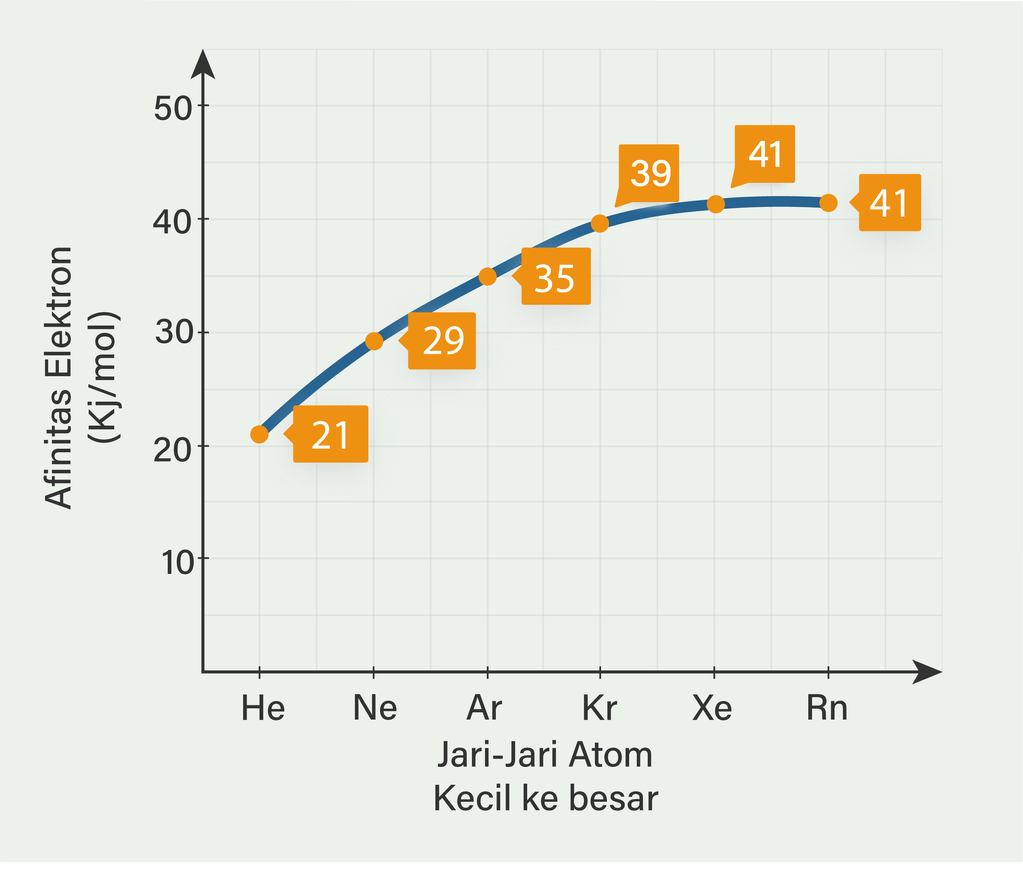
· 5.0 (1)
Iklan
DA
D. Aprilia
Mahasiswa/Alumni Universitas Pendidikan Indonesia
06 Maret 2022 09:47
Hai Nurul :) Jadi, grafik energi ionisasi terhadap jari-jari atom cenderung menurun, sedangkan grafik afinitas terhadap jari-jari atom cenderung meningkat. Perhatikan grafiknya pada gambar yaaa. Unsur pada golongan VIIIA disebut unsur gas mulia karena unsur ini sangat stabil (sukar bereaksi). Kestabilan ini karena konfigurasi elektron unsur gas mulia memenuhi aturan oktet (dan duplet untuk Helium). Unsur gas mulia terdapat sebagai molekul monoatomik. Kestabilannya juga dicerminkan dari energi ionisasinya yang sangat besar sedangkan afinitas nya sangat rendah. Dari tabel 3.4 diatas diketahui bahwa jari-jari atom dari atas ke bawah (He ke Rn) semakin besar. Begitu pula dengan afinitas elektronnya. Berikut data afinitas elektron unsur gas mulia dalam satuan kJ/mol : He = 21 Ne = 29 Ar = 35 Kr = 39 Xe = 41 Rn = 41 sehingga apabila kita gambarkan grafik afinitas terhadap jari-jari atom dari kecil ke besar, akan didapat grafik yang cenderung meningkat. Sedangkan untuk energi ionisasi semakin bawah semakin kecil, sehingga grafiknya terhadap jari-jari atom akan menurun.
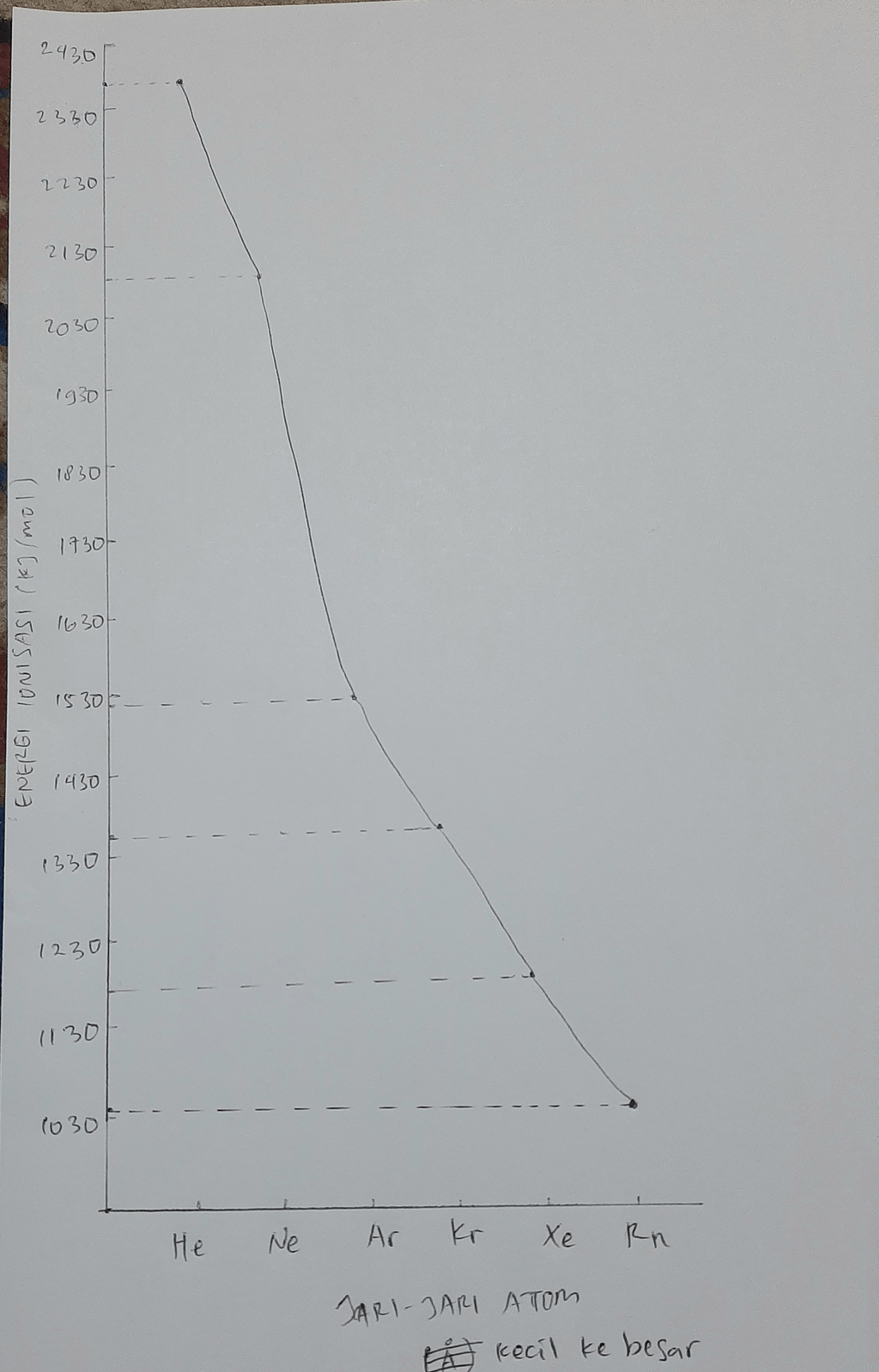
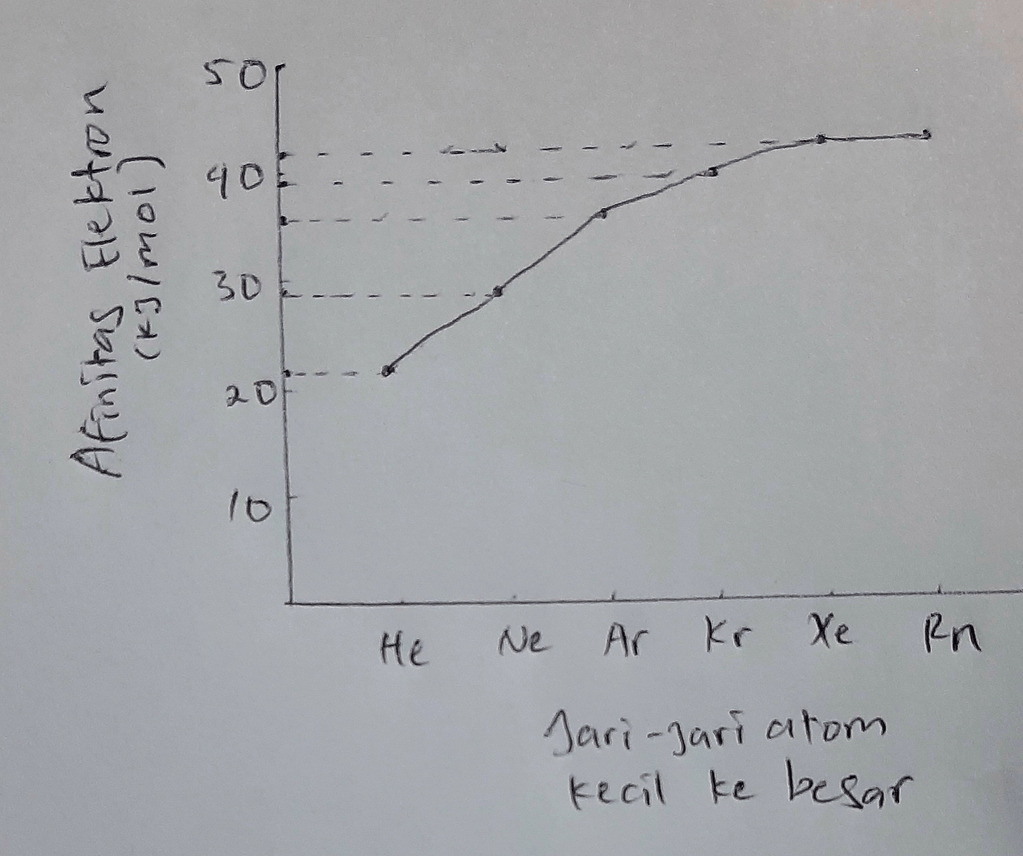
· 0.0 (0)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



