WW
Winn W
16 Februari 2021 13:44
Iklan
WW
Winn W
16 Februari 2021 13:44
Pertanyaan
besarnya konsentrasi ion H+ dalam 500ml larutan yang mengandung 5,50 gram kalium sulfida adalah...(ka H2s = 1,0 x 10-⁷ : A KB=39 g mol-¹ ,s =32 g mol-¹ dan H =1 g mol -¹)
29
4
Iklan
CY
C. Yudha
Mahasiswa/Alumni Politeknik Negeri Bandung
03 Januari 2022 14:30
Jawaban terverifikasi
Halo Winn, jawaban dari pertanyaan tersebut adalah 10^-10. Ayo simak pembahasan berikut agar kamu lebih paham ya^_^ Adanya ion H+ di dalam larutan menunjukan bahwa larutan tersebut bersifat asam. Semakin besar konsentrasi ion H+ yang ada di dalam larutan maka larutan akan semakin bersifat asam. K2S terbentuk dari basa kuat KOH dan asam lemah H2S dimana Ka H2S=10^-7. - Menentukan mol Kalium Sulifida (K2S) Mr K2S=110 gram/mol n K2S=massa K2S/ Mr K2S n K2S=5,5 gram/(110 gram/mol) n K2S=0,05 mol - Menentukan molaritas 500 mL=0,5 L M K2S=n H2S/Volume larutan M K2S=0,05/0,5 M K2S=0,1 mol/L - Menentukan konsentrasi H+ terlampir
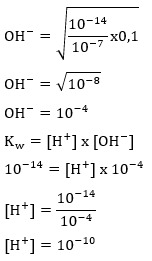
· 5.0 (3)
Iklan
LA
Luna A
18 Februari 2021 13:45
K₂S → 2K+ + S²¯ S²¯+2H₂O →H₂S + 2OH¯ 2K+ + H₂O → tidak ada reaksi (karena berasal dari Koh, basa kuat) Jadi, K₂S adalah garam basa Maka, [OH¯]= √Kw/Ka H₂S . [K₂S] = √10¯¹⁴/ 10¯⁷. n K₂S / V = √10¯¹⁴/ 10¯⁷. mK₂S / Mr K₂S/V = √10¯¹⁴/ 10¯⁷. 5,5 gr / (2×39 + 32) / 0,5L = √10¯¹⁴/ 10¯⁷. 5,5 gr / 110 / 0,5 L = √10¯¹⁴/ 10¯⁷. 10¯¹ = √10¯⁸ = 10¯⁴ Kw = [H+] × [OH¯] 10¯¹⁴ = [H+] × 10¯⁴ [H+] = 10¯¹⁴/ 10¯⁴ = 10¯¹⁰
· 5.0 (1)
WW
Winn W
16 Februari 2021 13:46
pliss dijawab atau gk rumus nya aj :)
· 0.0 (0)
EB
Eleven B
21 Februari 2021 04:08
10^-10
· 0.0 (0)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



