Icha N
28 Januari 2023 03:03
Iklan
Icha N
28 Januari 2023 03:03
Pertanyaan
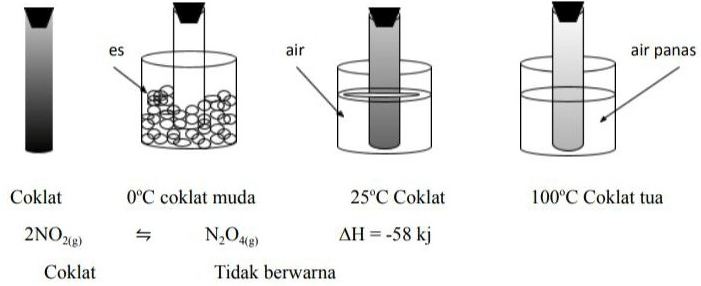
Berikut ini data percobaan reaksi kesetimbangan NO2 dan N2O4 pada berbagai suhu yang berbeda. Amati warna reaksi kesetimbangan pada tabung. Berdasarkan data di atas jawablah pertanyaan berikut! a) Pada reaksi di atas, kemana arah reaksi eksoterm dan endoterm?
2
1
Iklan
I. Qatrunnada
Mahasiswa/Alumni Univesitas Islam Indonesia
21 September 2023 10:24
<p>Jawaban : reaksi ke kanan (ke arah N<sub>2</sub>O<sub>4</sub>) bersifat eksoterm, dan reaksi ke kiri (ke arah 2NO<sub>2</sub> ) bersifat endoterm.</p><p> </p><p>Kesetimbangan kimia adalah keadaan saat kedua reaktan dan produk bertemu dalam konsentrasi yang tidak memiliki kecenderungan lebih lanjut untuk berubah seiring waktu.</p><p> </p><p>Entalpi adalah banyaknya energi yang mengalir, baik masuk atau keluar sistem pada kondisi tekanan tetap.</p><p> </p><p>Reaksi eksoterm merupakan reaksi yang melepas panas atau kalor, nilai ∆H = (-). Sedangkan reaksi endoterm, sistem akan menyerap energi dari lingkungan, nilai ∆H = (+)</p><p> </p><p>Pada reaksi diatas :</p><p>2NO<sub>2</sub> ⇌ N<sub>2</sub>O<sub>4</sub> ∆H =-58kJ</p><p>Dilihat dari nilai ∆H yang bernilai negatif, maka reaksi ke kanan bersifat eksoterm, dan reaksi ke kiri bersifat endoterm.</p><p> </p><p>Jadi, maka reaksi ke kanan (ke arah N<sub>2</sub>O<sub>4</sub>) bersifat eksoterm, dan reaksi ke kiri (ke arah 2NO<sub>2</sub> ) bersifat endoterm.</p>
Jawaban : reaksi ke kanan (ke arah N2O4) bersifat eksoterm, dan reaksi ke kiri (ke arah 2NO2 ) bersifat endoterm.
Kesetimbangan kimia adalah keadaan saat kedua reaktan dan produk bertemu dalam konsentrasi yang tidak memiliki kecenderungan lebih lanjut untuk berubah seiring waktu.
Entalpi adalah banyaknya energi yang mengalir, baik masuk atau keluar sistem pada kondisi tekanan tetap.
Reaksi eksoterm merupakan reaksi yang melepas panas atau kalor, nilai ∆H = (-). Sedangkan reaksi endoterm, sistem akan menyerap energi dari lingkungan, nilai ∆H = (+)
Pada reaksi diatas :
2NO2 ⇌ N2O4 ∆H =-58kJ
Dilihat dari nilai ∆H yang bernilai negatif, maka reaksi ke kanan bersifat eksoterm, dan reaksi ke kiri bersifat endoterm.
Jadi, maka reaksi ke kanan (ke arah N2O4) bersifat eksoterm, dan reaksi ke kiri (ke arah 2NO2 ) bersifat endoterm.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



