AM
Andi M
16 Juni 2022 10:56
Iklan
AM
Andi M
16 Juni 2022 10:56
Pertanyaan
Berikut ini beberapa pernyataan yang berhubungan dengan molekul H20, NH3, dan CH4. (1) Hibridisasi ketiga atom pusat molekul ini sama, yakni sp3. (2) Menurut model VSEPR: Hp bentuknya bengkok, NH3 bentuknya segitiga piramidal, dan CH4 bentuknya tetrahedral. (3) Tipe VSEPR untuk Hp: AX2E2; NH3: AX3E; dan CH4: AX4 (4) Atom pusat ketiga molekul ini hibridisasinya berbeda-beda, yaitu sp, sp2 , dan sp3. Pernyataan yang benar tentang molekul H2O, NH3, dan CH4 adalah (nomor atom C=6, N = 7, 0=8) (A) 1 , 2, dan 3 (D) hanya 4 (B) 1 dan 3 (E) 1, 2, 3, dan 4 (C) 2 dan 4
2
1
Iklan
Q'
Q. 'Ainillana
Mahasiswa/Alumni Universitas Negeri Yogyakarta
16 Juni 2022 15:28
Jawaban terverifikasi
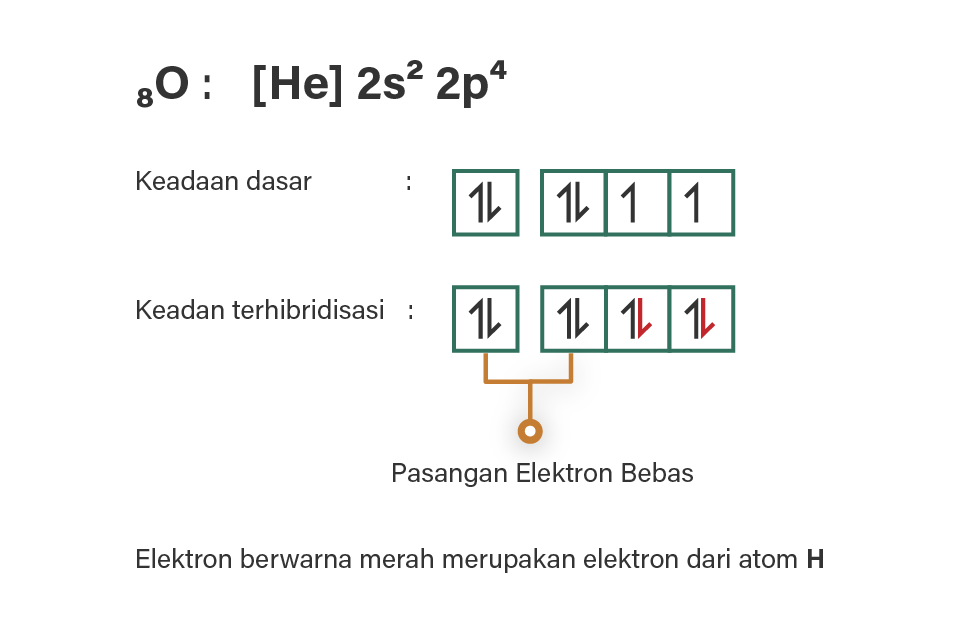
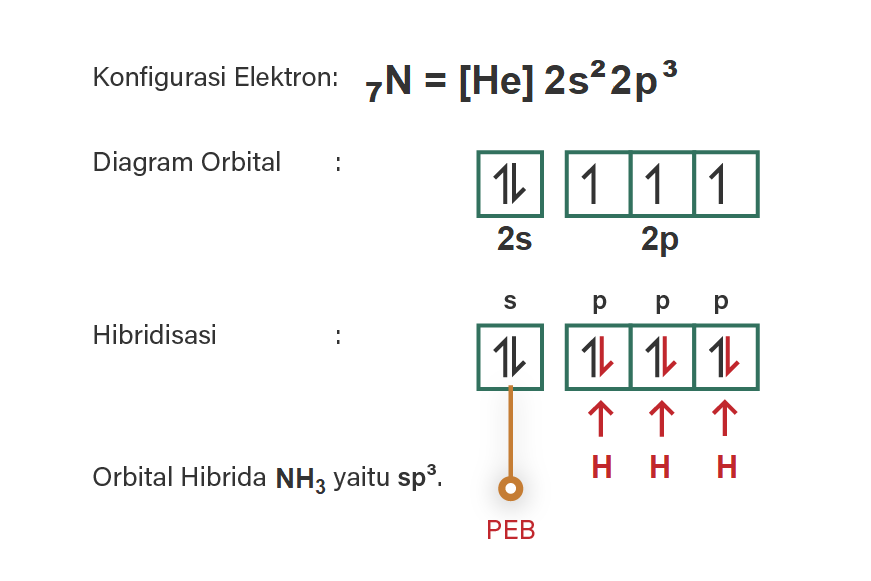
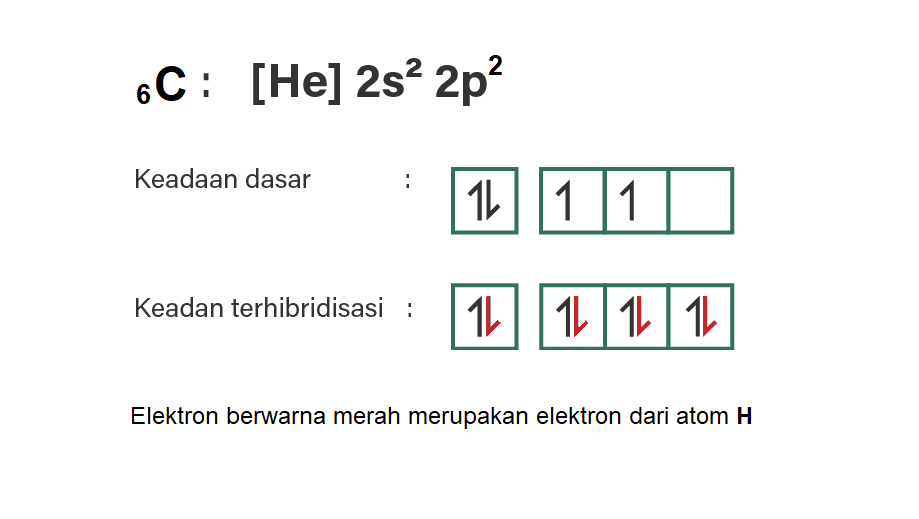
Jawaban yang benar untuk pertanyaan tersebut adalah A. Hibridisasi adalah peleburan orbital-orbital dari tingkat energi yang berbeda menjadi orbital-orbital yang energinya setingkat atau setara. Orbital yang dimaksud adalah orbital-orbital pada kulit terakhir atom yang berikatan. Untuk itu, perlu diketahui konfigurasi elektron atom-atom yang terlibat pada molekul tersebut. 1H = 1s1 (elektron valensi: 1) 8O = [He] 2s2 2p4 (elektron valensi: 6) 6C = [He] 2s2 2p2 (elektron valensi: 4) 7N = [He] 2s2 2p3 (elektron valensi: 5) Kemudian digambarkan diagram orbital masing-masing atom pusat, yaitu O, N, dan C. Pada molekul H2O terdapat dua atom H yang akan terikat pada atom O, 2 atom H tersebut dapat berikatan dengan dua elektron tunggal pada diagram orbital O. Pada molekul NH3, terdapat 3 elektron tunggal pada orbital p sehingga juga bisa ditempati 3 elektron dari atom H. Sedangkan pada molekul CH4, sepasang elektron dari 2s2 dieksitasi ke orbital 2p sehingga 4 elektron dari H dapat berpasangan dengan elektron dari atom C. Dengan demikian ketiga molekul memiliki hibridisasi atom pusat yang sama yaitu sp3. Namun, berdasarkan teori VSEPR ketiganya memiliki bentuk molekul berbeda. Hal ini disebabkan H2O memiliki 2 pasang elektron bebas, NH3 memiliki sepasang elektron bebas, sedangkan CH4 tidak memiliki pasangan elektron bebas. Perhatikan gambar, berturut-turut hibridisasi H2O, NH3, dan CH4. Ketiganya berturut-turut memiliki tipe molekul AX2E2, AX3E, dan AX4 yang mewakili bentuk molekul bengkok, segitiga piramidal, dan tetrahedral. Jadi, pernyataan yang benar tentang molekul H2O, NH3, dan CH4 adalah 1, 2, dan 3.
· 4.0 (2)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



