TT
Tira T
28 Maret 2022 16:18
Iklan
TT
Tira T
28 Maret 2022 16:18
Pertanyaan
Berdasarkan teori asam basa Lewis, manakah spesi yang bertindak sebagai asam dan basa? Jelaskan dengan menggunakan rumus elektron Lewis! 9. NH2^- + H+ ➝ NH3
1
1
Iklan
Q'
Q. 'Ainillana
Mahasiswa/Alumni Universitas Negeri Yogyakarta
29 Maret 2022 14:40
Jawaban terverifikasi
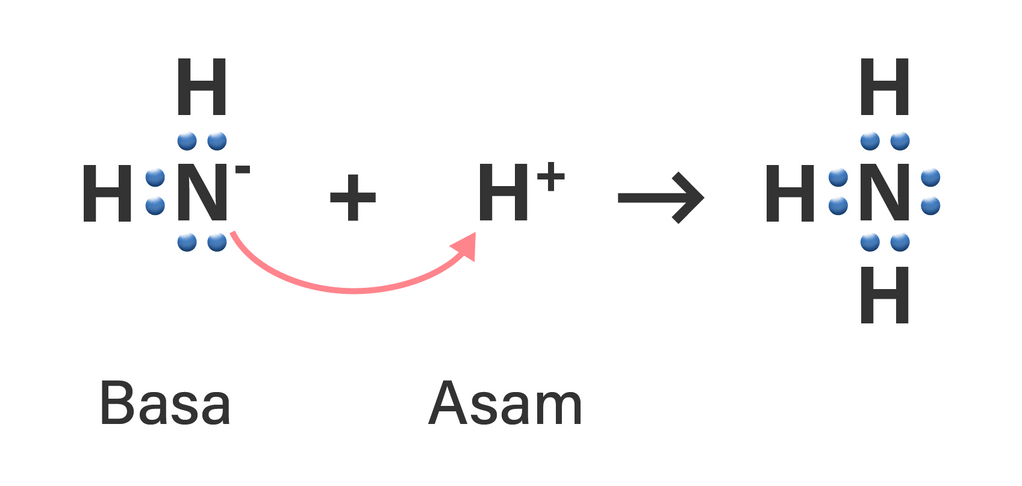
Halo Tira T, spesi yang bertindak sebagai asam Lewis adalah H+, sedangkan yang bertindak sebagai basa adalah NH2-. Agar lebih jelas, simak pembahasan berikut yaa :) Menurut Lewis, basa adalah spesi yang dapat mendonorkan pasangan elektron bebas kepada pasangan reaksinya, sedangkan asam adalah spesi yang menerima pasangan elektron bebas tersebut. Untuk itu, kita perlu gambarkan struktur Lewis ion NH2-, ion H+, dan molekul NH3. Perhatikan pada gambar terlampir, bahwa ion NH2- memiliki 2 pasangan elektron bebas yang dapat didonorkan kepada H+ yang tidak mempunyai pasangan elektron sama sekali. Sehingga, NH2- merupakan basa dan H+ adalah asam menurut Lewis. Terimakasih telah bertanya di Roboguru, semoga terbantu :D
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



