RR
Rahayu R
05 Februari 2022 15:19
Iklan
RR
Rahayu R
05 Februari 2022 15:19
Pertanyaan
Berdasarkan persamaan kimia untuk reaksi-reaksi berikut: Pasangan yang bukan merupakan pasangan asam-basa konjugasi adalah… (A) CH3OH dan CH3O^- (B) HC2H3O2 dan CH3O^- (C) C6H5NH2 dan C6H5NH3^+ (D) C2H3O2^- dan HC2H3O2 (E) HCO3^- dan CO3^2-
1
1
Iklan
MB
M. Bimba
Mahasiswa/Alumni Universitas Sanata Dharma
11 Februari 2022 17:59
Jawaban terverifikasi
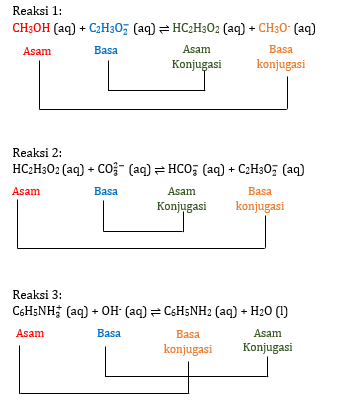
Hai Rahayu R, kakak bantu jawab ya 😁 Jadi, yang bukan pasangan asam-basa konjugasi adalah B. HC2H3O2 dan CH3O^- Ayo simak penjelasan berikut, supaya lebih paham^^ Pada teori asam basa yang dikemukakan oleh Bronsted-Lowry, dijelaskan bahwa reaksi asam dan basa dapat terjadi karena tranfer proton (H+). Oleh sebab itu, Bronsted-Lowry menyatakan bahwa asam merupakan spesi pendonor proton dan basa merupakan spesi penerima proton. Pada teori ini, terdapat istilah asam konjugasi dan basa konjugasi. Menurut Bronsted-Lowry, asam konjugasi merupakan senyawa yang terbentuk dari basa yang telah menerima proton. Sedangkan, basa konjugasi merupakan senyawa yang terbentuk dari asam yang telah mendonorkan protonnya. Untuk menentukan pasangan asam-basa konjugasinya, maka dari masing-masing reaksi ditentukan terlebih dahulu spesi yang bertindak sebagai asam, basa, lalu asam konjugasi, dan basa konjugasi. Berikut penentuannya dapat dilihat pada gambar terlampir. Untuk menentukan pasangan asam-basa konjugasi dapat dilihat berdasarkan senyawa yang memiliki rumus kimia yang hampir sama. Pada reaksi 1, senyawa CH3OH sebelum bereaksi memiliki satu proton, setelah bereaksi CH3OH kehilangan protonnya untuk membentuk ion CH3O-. Oleh sebab itu, CH3OH akan mendonorkan proton kepada ion C2H3O_2^-. Maka, senyawa C2H3O_2^- akan menerima proton untuk membentuk HC2H3O2. Dengan demikian, CH3OH akan bertindak sebagai asam dan ion CH3O- sebagai basa konjugasi, sedangkan ion C2H3O_2^- bertindak sebagai basa dan HC2H3O2 bertindak sebagai asam konjugasi. Maka pasangan asam basa konjugasinya adalah CH3OH dengan CH3O- atau C2H3O_2^- dengan HC2H3O2. Untuk menentukan pasangan asam-basa konjugasi dapat dilihat berdasarkan senyawa yang memiliki rumus kimia yang hampir sama. Pada reaksi 2, senyawa HC2H3O2 sebelum bereaksi memiliki satu proton, setelah bereaksi HC2H3O2 kehilangan protonnya untuk membentuk ion C2H3O_2^-. Oleh sebab itu, HC2H3O2 akan mendonorkan proton kepada ion CO_3^(2-). Maka, senyawa ion CO_3^(2-) akan menerima proton untuk membentuk ion HCO_3^-. Dengan demikian, HC2H3O2 akan bertindak sebagai asam dan ion C2H3O_2^- sebagai basa konjugasi, sedangkan ion CO_3^(2-) bertindak sebagai basa dan HCO_3^- bertindak sebagai asam konjugasi. Maka pasangan asam basa konjugasinya adalah CO_3^(2-) dengan HCO_3^- atau C2H3O_2^- dengan HC2H3O2. Untuk menentukan pasangan asam-basa konjugasi dapat dilihat berdasarkan senyawa yang memiliki rumus kimia yang hampir sama. Pada reaksi 3, senyawa C6H5NH_3^+ sebelum bereaksi memiliki tiga proton, setelah bereaksi C6H5NH_3^+ kehilangan protonnya untuk membentuk C6H5NH2. Oleh sebab itu, C6H5NH_3^+ akan mendonorkan proton kepada ion OH-. Maka, ion OH- akan menerima proton untuk membentuk H2O. Dengan demikian, C6H5NH_3^+ akan bertindak sebagai asam dan C6H5NH2 sebagai basa konjugasi, sedangkan ion OH- bertindak sebagai basa dan H2O bertindak sebagai asam konjugasi. Maka pasangan asam basa konjugasinya adalah C6H5NH_3^+ dengan C6H5NH2 atau OH- dengan H2O. Semoga membantu ya. Selamat belajar 😎
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



