Dtpm D
16 Agustus 2022 17:36
Iklan
Dtpm D
16 Agustus 2022 17:36
Pertanyaan
bagaimana cara membedakan senyawa 1-butanol dengan 2-butanol
2
1
Iklan
D. Aprilia
Mahasiswa/Alumni Universitas Pendidikan Indonesia
07 Oktober 2022 04:30
<p>Jawaban: mengoksidasi kedua larutan, atau bisa dengan uji Lucas, atau dengan mengukur titik didihnya.</p><p> </p><p>Alkohol termasuk senyawa turunan alkana yang mengandung gugus fungsi –OH.</p><p>Berdasarkan letak terikatnya gugus –OH , senyawa alkohol dibedakan menjadi :</p><p>1. Alkohol primer (gugus –OH terikat pada atom C primer)</p><p>2. Alkohol sekunder (gugus –OH terikat pada atom C sekunder)</p><p>3. Alkohol tersier (gugus –OH terikat pada atom C tersier)</p><p> </p><p>1-butanol merupakan alkohol primer, sedangkan 2-butanol termasuk alkohol sekunder. (perhatikan gambar)</p><p> </p><p>Kedua senyawa alkohol ini memiliki jumlah atom C yang sama. Untuk membedakan alkohol primer dan alkohol sekunder salah satunya yaitu dengan cara mengoksidasi kedua senyawa tersebut menggunakan oksidator kuat seperti KMnO<sub>4</sub> atau K<sub>2</sub>Cr<sub>2</sub>O<sub>7</sub>.</p><p> </p><p>Oksidasi alkohol primer akan menghasilkan aldehid, dan jika dioksidasi lebih lanjut akan menghasilkan asam karboksilat.</p><p>Reaksi oksidasi tahap 1 dari 1-butanol menghasilkan butanal (aldehid), dan apabila butanal ini dioksidasi lebih lanjut akan menghasilkan asam butanoat (Asam karboksilat).</p><p> </p><p>Sedangkan apabila alkohol sekunder dioksidasi akan menghasilkan senyawa keton. Reaksi oksidasi 2-butanol menghasilkan senyawa 2-butanon.</p><p> </p><p>Cara selanjutnya untuk membedakan alkohol primer dan sekunder di laboratorium yaitu dengan uji Lucas.</p><p>Pereaksi yang digunakan adalah larutan HCl pekat dan katalis ZnCl<sub>2</sub>. Dalam uji Lucas ini menghasilkan gelembung gas.</p><p>Perbedaannya, alkohol primer bereaksi sangat lambat sehingga gelembung gas yang dihasilkan lebih lama. Sedangkan alkohol sekunder bereaksi lebih cepat dalam menghasilkan gelembung gas.</p><p> </p><p>Selain itu, bisa juga dengan mendidihkan kedua larutan. Alkohol primer memiliki titik didih lebih tinggi dibanding alkohol sekunder.</p><p>1-butanol = 118<sup>o</sup>C</p><p>2-butanol = 100<sup>o</sup>C</p><p> </p><p>Jadi, untuk membedakan 1-butanol dengan 2-butanol bisa dengan cara mengoksidasinya, dengan uji Lucas, atau dengan mengukur titik didihnya.</p>
Jawaban: mengoksidasi kedua larutan, atau bisa dengan uji Lucas, atau dengan mengukur titik didihnya.
Alkohol termasuk senyawa turunan alkana yang mengandung gugus fungsi –OH.
Berdasarkan letak terikatnya gugus –OH , senyawa alkohol dibedakan menjadi :
1. Alkohol primer (gugus –OH terikat pada atom C primer)
2. Alkohol sekunder (gugus –OH terikat pada atom C sekunder)
3. Alkohol tersier (gugus –OH terikat pada atom C tersier)
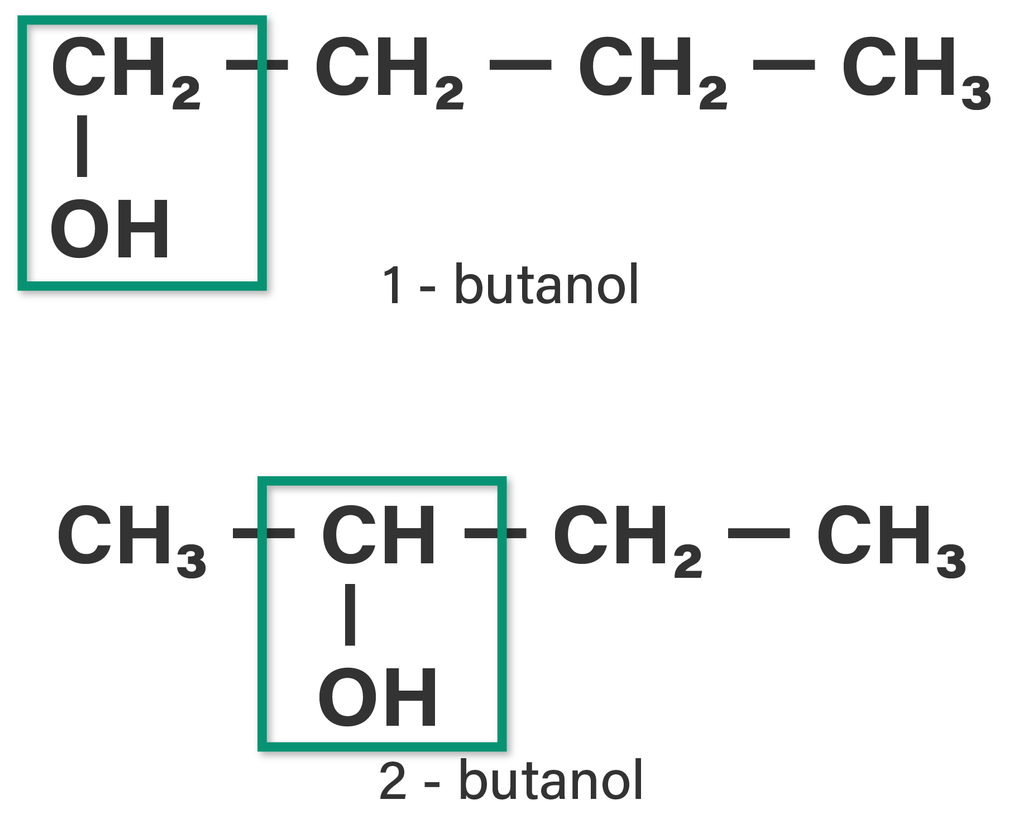
1-butanol merupakan alkohol primer, sedangkan 2-butanol termasuk alkohol sekunder. (perhatikan gambar)
Kedua senyawa alkohol ini memiliki jumlah atom C yang sama. Untuk membedakan alkohol primer dan alkohol sekunder salah satunya yaitu dengan cara mengoksidasi kedua senyawa tersebut menggunakan oksidator kuat seperti KMnO4 atau K2Cr2O7.
Oksidasi alkohol primer akan menghasilkan aldehid, dan jika dioksidasi lebih lanjut akan menghasilkan asam karboksilat.
Reaksi oksidasi tahap 1 dari 1-butanol menghasilkan butanal (aldehid), dan apabila butanal ini dioksidasi lebih lanjut akan menghasilkan asam butanoat (Asam karboksilat).
Sedangkan apabila alkohol sekunder dioksidasi akan menghasilkan senyawa keton. Reaksi oksidasi 2-butanol menghasilkan senyawa 2-butanon.
Cara selanjutnya untuk membedakan alkohol primer dan sekunder di laboratorium yaitu dengan uji Lucas.
Pereaksi yang digunakan adalah larutan HCl pekat dan katalis ZnCl2. Dalam uji Lucas ini menghasilkan gelembung gas.
Perbedaannya, alkohol primer bereaksi sangat lambat sehingga gelembung gas yang dihasilkan lebih lama. Sedangkan alkohol sekunder bereaksi lebih cepat dalam menghasilkan gelembung gas.
Selain itu, bisa juga dengan mendidihkan kedua larutan. Alkohol primer memiliki titik didih lebih tinggi dibanding alkohol sekunder.
1-butanol = 118oC
2-butanol = 100oC
Jadi, untuk membedakan 1-butanol dengan 2-butanol bisa dengan cara mengoksidasinya, dengan uji Lucas, atau dengan mengukur titik didihnya.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



