IF
Indah F
18 Januari 2020 11:01
Iklan
Iklan
IF
Indah F
18 Januari 2020 11:01
22
1
Iklan
Iklan
CY
C. Yudha
Mahasiswa/Alumni Politeknik Negeri Bandung
22 Desember 2021 13:23
Jawaban terverifikasi
Halo Indah, jawaban dari pertanyaan tersebut adalah 0,00632. Ayo simak pembahasan berikut agar kamu lebih paham ya^_^ Derajat disosiasi berada pada rentang 0-1. Pada dasarnya semakin besar derajat disosiasi maka senyawa tersebut akan terurai secara sempurna di dalam air. Kemudian jika derajat disosiasinya kecil menunjukan senyawa tersebut tidak terurai secara sempurna menjadi ion-ion penyusunnya. Derajat disosiasi yang kecil mengindikasikan bahwa senyawa tersebut sebagai senyawa elektrolit lemah. Asam asetat jika terdisosiasi dalam air akan menghasilkan ion (terlampir). Disosiasi asam asetat tersebut menghasilkan dua ion yaitu CH3COO- dan H+ sehingga nanti ketika sudah menemukan konsentrasi salah satu ionnya maka harus dijumlahkan dengan ion yang ada. Untuk menjawab soal ini maka lakukanlah perhitungan dengan asumsi sebagai awal perhitungan menggunakan ion H+ sebagai ion terlarutnya. [Disosiasi]=[ion terlarut]xderajat disosiasi [H+]=[1 M]x0,316% [H+]=0,00316 M Karena koefisien CH3COO- sama dengan koefisien H+ sehingga [CH3COO-]=[H+]=0,00316 M. Nah karena terdapat dua ion tersebutlah konsentrasi ionnya harus dijumlahkan [Konsentrasi total ion]=0,00316 + 0,00316 [Konsentrasi total ion]=0,00632 M.
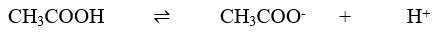
· 0.0 (0)
Iklan
Iklan

Yah, akses pembahasan gratismu habis
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke Forum
Biar Robosquad lain yang jawab soal kamu

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!


