RN
Rahma N
19 November 2021 06:56
Iklan
RN
Rahma N
19 November 2021 06:56
Pertanyaan
90th bohr golongan dan periode unsur beserta mekanika kuantum
2
1
Iklan
NB
N. Badiani
16 Januari 2022 13:22
Jawaban terverifikasi
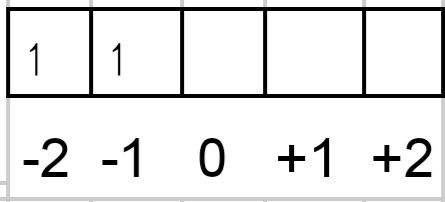
Hai Rahma, kakak bantu jawab ya. Jawaban dari pertanyaan kamu adalah Konfigurasi elektron dari ₉₀Th : [Rn] 7s² 6d² Periode : 7 Golongan : Aktinida Bilangan kuantum : n = 6, l = 2, m = -1, s = + 1/2 Simak penjelasan kakak ya. Konfigurasi elektron merupakan penataan elektron pada kulit atom. Untuk nomor atom yang relatif besar, konfigurasi elektron dapat disingkat menggunakan unsur gas mulia. ₂[He] 2s dan seterusnya ₁₀[Ne] 3s dan seterusnya ₁₈[Ar] 4s dan seterusnya ₃₆[Kr] 5s dan seterusnya ₅₄[Xe] 6s dan seterusnya ₈₆[Rn] 7s dan seterusnya Dalam soal ditanyakan konfigurasi elketron dari ₉₀Th. Karena nomor atomnya 90, maka unsur gas mulia terdekat adalah Rn dengan nomor atom 86. Sehingga konfigurasi ₉₀Th sebagai berikut. ₉₀Th : [Rn] 7s² 5f² Namun, pada kenyataanya terjadi penyimpangan pada ubkulit 5f. Elektron yang seharusnya berada pada subkulit 5f, menempati subkulit 6d. Hal ini disebabkan tingat energi yang mirip antara 5f dengan 6d, sehingga elektron dapat berpindah. Maka dari itu, konfigurasi dari ₉₀Th : [Rn] 7s² 6d². Untuk menentukan letak periode suatu unsur, dilihat dari kulit terbesar yang ditempati oleh elektron. Pada ₉₀Th : [Rn] 7s² 6d², kulit terbesar adalah kulit 7, maka Th terletak pada periode 7. Karena sebenarnya konfigurasi Th berakhir pada subkulit 5f, maka Th terletak pada golongan aktinida. Bilangan kuantum merupakan identitas elektron yang menunjukkan keberadaan elektron. Bilangan kuantum terdapat empat jenis, yaitu : 1. Bilangan kuantum utama (n), menunjukkan kulit dimana elektron yang dimaksud berada. 2. Bilangan kuantum azimut (l), menunjukkan subkulit dimana elektrn tersebut berada. 3. Bilangan kuantum elektron magnetik (m), menunjukkan posisi elektron pada orbital 4. Bilangan kuantum spin (s), menunjukan arah perputaran elektron. Pada ₉₀Th : [Rn] 7s² 6d², jika ditanyakan bilangan kuantum elektron terakhir, maka elektron pada 6d² lah yang kita identifikasi. Dari 6d², maka : 1. n = kulit = 6 2. l = subkulit, aturannya : subkulit s, l = 0 subkulit p, l = 1 subkulit d, l = 2 Karena pada Th elektron terakhir berada pada 6d², maka nilai l = 2 3. m = letak pada orbital, aturannya subkulit s memiliki 1 orbital subkulit p memiliki 3 orbital subkulilt d memiliki 5 orbital. Untuk penentuan nilai m, lihat lampiran. 4. s = arah perputaran +1/2 jika searah jarum jam (↿) -1/2 jika berlawanan arah jarum jam (⇂) Karena elektron searah jarum jam (bisa lihat lampiran), maka s = + 1/2. Dari uraian di atas, dapat disimpulkan bahwa : Konfigurasi elektron dari ₉₀Th : [Rn] 7s² 6d² Periode : 7 Golongan : Aktinida Bilangan kuantum : n = 6, l = 2, m = -1, s = + 1/2 Terimakasih sudah bertanya pada roboguru, semoga bermanfaat.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



