AA
Ana A
06 April 2022 05:11
Iklan
AA
Ana A
06 April 2022 05:11
Pertanyaan
100ml larutan H2SO4 0,002M dicampur dengan 100ml larutan naoh yang ph nya = 11. ph campuran yang terjadi adalah .... A.3−log1 B.3−log2 C.1−log3 D.2−log3 E.3−log3
1
1
Iklan
YL
Y. Lutvira
01 Agustus 2022 04:24
Jawaban terverifikasi
Jawaban yang benar adalah A pH adalah derajat keasaman untuk menentukan tingkat keasaman/kebasaan suatu larutan. Menentukan mol H2SO4 mol = molaritas x volume mol = 0,002 M x 100 mL mol = 0,2 mmol Menentukan pOH NaOH pH = 11 pOH = 14 - pH pOH = 14 - 11 pOH = 3 Menentukan [OH-] dari NaOH pOH = - log [OH-] 3 = - log [OH-] [OH-] = 10⁻³ M Menentukan konsentrasi dari NaOH Valensi basa NaOH sama dengan jumlah ion OH-, yaitu 1 [OH-] = M x valensi basa 10⁻³ = M x 1 M = 10⁻³ M Menentukan mol NaOH mol = Molaritas x volume mol = 10⁻³ M x 100 mL mol = 0,1 mmol Mol mrs terlampir yang masih bersisa adalah H2SO4, jadi perhitungan M menggunakan rumus: Molaritas = mol/volume total Molaritas = 0,1 mmol/200 mL Molaritas = 5 x 10⁻⁴ M Menentukan [H+] valensi asam H2SO4 sama dengan jumlah ion H+nya yaitu 2 [H+] = 5 x 10⁻⁴ M x 2 [H+] = 1 x 10⁻³ M Menentukan pH pH = - log[H+] pH = - log 1 x 10⁻³ pH = 3 Jadi pH yang didapat adalah 3
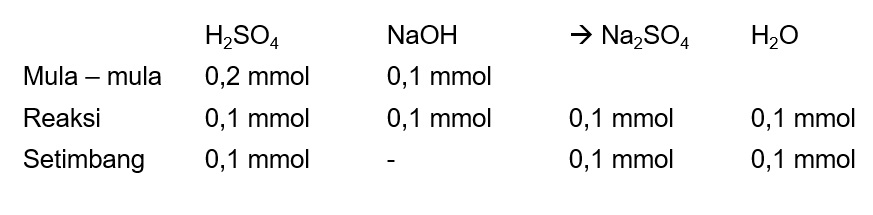
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



