AM
Andi M
06 Juni 2022 02:05
Iklan
AM
Andi M
06 Juni 2022 02:05
Pertanyaan
1 mmol propanol + 10 ml asam asetat + 10 tetes asam sulfat pekat jika produk utama yang terbentuk sebanyak 0,74 gram rendemen produk yang dihasilkan sebesar
7
1
Iklan
AA
A. Anania
Mahasiswa/Alumni Hanyang University
09 Juni 2022 08:29
Jawaban terverifikasi
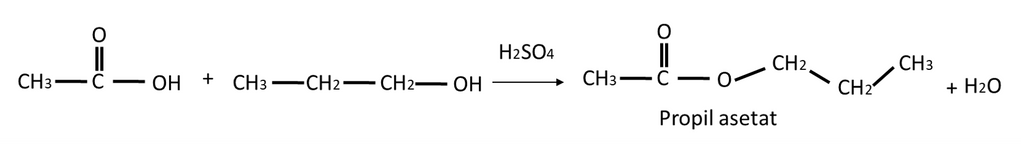
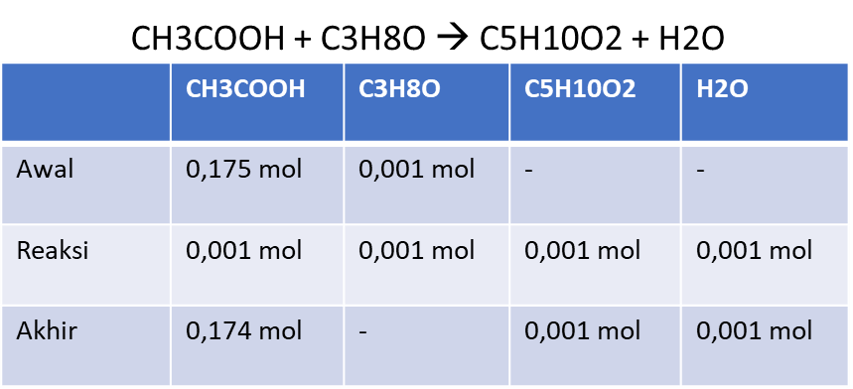
Jawaban yang tepat adalah 725,5%. Propanol adalah senyawa alkohol dengan rumus CH3-CH2-CH2-OH, sedangkan asam asetat adalah senyawa asam karboksilat dengan rumus CH3-CH2-COOH. Reaksi yang terjadi antara alkohol dengan asam karboksilat dalam suasana asam adalah reaksi esterifikasi, yaitu reaksi pembentukan senyawa ester. Senyawa ester memiliki rumus umum R-COO-R’. Reaksi yang terjadi antara propanol dan asam asetat dengan katalis asam sulfat adalah seperti pada gambar dibawah ini. Produk yang dihasilkan adalah propil asetat dengan rumus umum C5H10O2. Untuk menghitung rendemen produk yang dihasilkan, kita perlu menghitung berapa mol propil asetat yang dihasilkan secara teori. Diketahui propanol yang tersedia sebanyak 1 mmol, sedangkan asam asetat sebanyak 10 ml. Asam asetat memiliki berat jenis 1,05 g/ml. Jadi, massa asam asetat yang digunakan adalah: Massa asam asetat = volume x berat jenis Massa asam asetat = 10 ml x 1,05 g/ml Massa asam asetat = 10,5 g Mol asam asetat = massa / Mr asam asetat Mol asam asetat = 10,5 g/ ((2x12)+(4x1)+(2x16))g/mol Mol asam asetat = 10,5 g / 60 g/mol Mol asam asetat = 0,175 mol Kemudian kita dapat menghitung berapa mol propil asetat yang dihasilkan secara teori. Perhitungannya seperti pada gambar dibawah ini. Jadi, secara teori, propil asetat yang dihasilkan adalah sebanyak 0,001 mol. Kita dapat menghitung massa-nya dengan cara berikut: Massa propil asetat = mol x Mr Massa propil asetat = 0,001 mol x ((5x12)+(10x1)+(2x16)) g/mol Massa propil asetat = 0,001 mol x 102 g/mol Massa propil asetat = 0,102 g Dalam soal diketahui bahwa propil asetat yang terbentuk adalah sebanyak 0,74 g, maka rendemen produk adalah: Rendemen produk = (massa produk yang terbentuk/massa teoritis) x 100% Rendemen produk = (0,74 g/0,102 g) x 100% Rendemen produk = 725,5% Jadi, rendemen produk yang dihasilkan dari reaksi tersebut adalah sebanyak 725,5%.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



