Ohhh A
29 Juli 2024 02:50
Iklan
Ohhh A
29 Juli 2024 02:50
Pertanyaan
tekanan uap air pada 25° c adakah 25 atm berapakh teknan uap suatu larutan padav25° c yang dibuat dgn melarutkan 0,5 mol sukrosa adalah 12 mol air
1
2
Iklan
Hartila S
29 Juli 2024 05:17
<p>Jawaban terlampir</p>
Jawaban terlampir
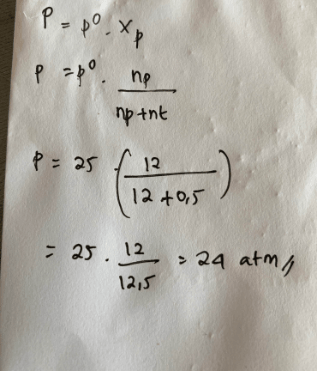
· 5.0 (1)
Iklan
J. Siregar
30 Juli 2024 00:41
<p>Jawabannya adalah tekanan uap larutan (P) = 24 atm.</p><p> </p><p>Tekanan uap larutan (P) dapat dihitung dengan menggunakan hukum Roult.</p><p>P = Xp . P°</p><p>P = (np/nt+np) . P°</p><p>keterangan:</p><p>P° = tekanan uap jenuh pelarut murni</p><p>Xp = fraksi mol pelarut</p><p>nt = mol terlarut</p><p>np = mol pelarut</p><p> </p><p>Berdasarkan data soal, sukrosa terlarut dalam air.</p><p>P° = 25 atm</p><p>nt = 0,5 mol</p><p>np = 12 mol</p><p>P = Xp . P°</p><p>P = (np/nt+np) . P°</p><p>P = 12 mol/(0,5 mol + 12 mol) . 25 atm</p><p>P = 24 atm</p><p> </p><p>Jadi, tekana uap larutan sukrosa sebesar 24 atm.</p>
Jawabannya adalah tekanan uap larutan (P) = 24 atm.
Tekanan uap larutan (P) dapat dihitung dengan menggunakan hukum Roult.
P = Xp . P°
P = (np/nt+np) . P°
keterangan:
P° = tekanan uap jenuh pelarut murni
Xp = fraksi mol pelarut
nt = mol terlarut
np = mol pelarut
Berdasarkan data soal, sukrosa terlarut dalam air.
P° = 25 atm
nt = 0,5 mol
np = 12 mol
P = Xp . P°
P = (np/nt+np) . P°
P = 12 mol/(0,5 mol + 12 mol) . 25 atm
P = 24 atm
Jadi, tekana uap larutan sukrosa sebesar 24 atm.
· 5.0 (1)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



