Nadin A
22 Mei 2022 05:25
Iklan
Nadin A
22 Mei 2022 05:25
Pertanyaan
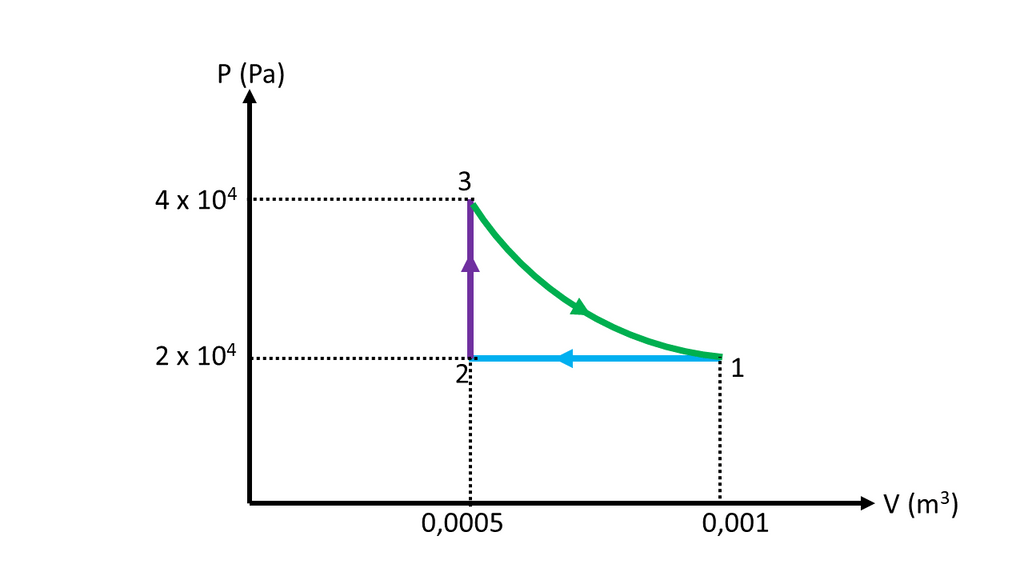
Suatu gas ideal mula-mula suhunya 400 K, tekanan 2×10^4 Pa dan volumenya 0.001m^(3). Gas dikompesi secara perlahan pada tekanan konstan ditekan sehingga volumenya menjadi separuh semula. kemudian kalor ditambahkan ke gas sementara volume diatur tetap konstan sehingga suhu dan tekanan naik sampai suhu sama dengan suha mula- mula. Sistem kemudian diekspansi pada suhu tetap sehingga volumenya sama dengan mula -mula. Gambarkan proses – proses tersebut dalam suatu diagram P-V!
2
3
Iklan
V. Shavira
31 Januari 2023 13:10
<p>Jawaban yang benar dapat dilihat pada gambar.</p><p> </p><p>Diketahui:</p><p>suhu kondisi 1 --> T1 = 400 K</p><p>tekanan kondisi 1 --> P1 = 2 x 10<sup>4</sup> Pa</p><p>volume kondisi 1 --> V1 = 0,001 m<sup>3</sup></p><p>suhu kondisi 2 --> T2 = ..?</p><p>tekanan kondisi 2 --> P2 = P1 = 2 x 10<sup>4</sup> Pa</p><p>volume kondisi 2 --> V2 = V1/2 = 0,001/2 = 0,0005 m<sup>3</sup></p><p>suhu kondisi 3 --> T3 = T1 = 400 K</p><p>tekanan kondisi 3 --> P3 = ?</p><p>volume kondisi 3 --> V3 = V2 = 0,0005 m<sup>3</sup></p><p>suhu kondisi 4 --> T4 = T1 = 400 K</p><p>tekanan kondisi 4 --> P4 = ?</p><p>volume kondisi 4 --> V4 = V1 = 0,0005 m<sup>3</sup></p><p> </p><p>Ditanya : Diagram P-V?</p><p>Jawab:</p><p>(1) Kita cari dulu suhu pada kondisi 2 dengan menggunakan persamaan Hukum Charles untuk proses 1 ke 2</p><p>V1 / T1 = V2 / T2</p><p>0,001 / 400 = 0,0005 / T2</p><p>T2 = 200 K</p><p>(2) Kita cari tekanan pada kondisi 3 dengan menggunakan persamaan Hukum Gay-Lussac untuk proses 2 ke 3</p><p>P2 / T2 = P3 / T3</p><p>2 x 10<sup>4</sup> / 200 = P3 / 400</p><p>P3 = 4 x 10<sup>4</sup> Pa</p><p>(3) Kita cari tekanan pada kondisi 4 dengan persamaan Hukum Boyle untuk proses 3 ke 4</p><p>P3*V3 = P4*V4</p><p>4 x 10<sup>4</sup> *0,0005 = P4 * 0,001</p><p>P4 = 2 x 10<sup>4</sup> Pa</p><p> </p><p>Karena tekanan pada kondisi 4 dan kondisi 1 adalah sama, dan volume pada kondisi 4 dan 1 adalah sama, maka kondisi 4 ternyata sama dengan kondisi 1. Sehingga, diagram P-V untuk proses tersebut dapat dilihat pada gambar.</p><p> </p><p>Jadi, gambar proses – proses tersebut dalam suatu diagram P-V dapat dilihat pada gambar terlampir</p><p> </p>
Jawaban yang benar dapat dilihat pada gambar.
Diketahui:
suhu kondisi 1 --> T1 = 400 K
tekanan kondisi 1 --> P1 = 2 x 104 Pa
volume kondisi 1 --> V1 = 0,001 m3
suhu kondisi 2 --> T2 = ..?
tekanan kondisi 2 --> P2 = P1 = 2 x 104 Pa
volume kondisi 2 --> V2 = V1/2 = 0,001/2 = 0,0005 m3
suhu kondisi 3 --> T3 = T1 = 400 K
tekanan kondisi 3 --> P3 = ?
volume kondisi 3 --> V3 = V2 = 0,0005 m3
suhu kondisi 4 --> T4 = T1 = 400 K
tekanan kondisi 4 --> P4 = ?
volume kondisi 4 --> V4 = V1 = 0,0005 m3
Ditanya : Diagram P-V?
Jawab:
(1) Kita cari dulu suhu pada kondisi 2 dengan menggunakan persamaan Hukum Charles untuk proses 1 ke 2
V1 / T1 = V2 / T2
0,001 / 400 = 0,0005 / T2
T2 = 200 K
(2) Kita cari tekanan pada kondisi 3 dengan menggunakan persamaan Hukum Gay-Lussac untuk proses 2 ke 3
P2 / T2 = P3 / T3
2 x 104 / 200 = P3 / 400
P3 = 4 x 104 Pa
(3) Kita cari tekanan pada kondisi 4 dengan persamaan Hukum Boyle untuk proses 3 ke 4
P3*V3 = P4*V4
4 x 104 *0,0005 = P4 * 0,001
P4 = 2 x 104 Pa
Karena tekanan pada kondisi 4 dan kondisi 1 adalah sama, dan volume pada kondisi 4 dan 1 adalah sama, maka kondisi 4 ternyata sama dengan kondisi 1. Sehingga, diagram P-V untuk proses tersebut dapat dilihat pada gambar.
Jadi, gambar proses – proses tersebut dalam suatu diagram P-V dapat dilihat pada gambar terlampir
· 4.0 (2)
Iklan
DAHLIA D
25 Februari 2024 12:12
Reaktor batch volume konstan 200 L dengan tekanan 20 atm, mengandung 75% senyawa A dan 25% inert. Reaksi fase gas terjadi secara isothermal pada suhu 227 deg * C • Reaksi: A -> B + C • Jika diasumsikan hukum gas ideal berlaku pada kondisi ini, berapa mol A terbentuk dalam reaktor mula-mula? • Jika reaksi orde 1: - r_{A} = k*C_{A} dengan k = 0 ,1/menit, hitung waktu yang dibutuhkan untuk mengkonsumsi 99% A! • Jika reaksi orde 2: - r_{A} = k*C_{A} ^ 2 dengan k= 0.7L / m * ol /menit hitung waktu yang dibutuhkan untuk mengkonsumsi 80% A!
· 0.0 (0)
DAHLIA D
25 Februari 2024 12:12
Reaktor batch volume konstan 200 L dengan tekanan 20 atm, mengandung 75% senyawa A dan 25% inert. Reaksi fase gas terjadi secara isothermal pada suhu 227 deg * C • Reaksi: A -> B + C • Jika diasumsikan hukum gas ideal berlaku pada kondisi ini, berapa mol A terbentuk dalam reaktor mula-mula? • Jika reaksi orde 1: - r_{A} = k*C_{A} dengan k = 0 ,1/menit, hitung waktu yang dibutuhkan untuk mengkonsumsi 99% A! • Jika reaksi orde 2: - r_{A} = k*C_{A} ^ 2 dengan k= 0.7L / m * ol /menit hitung waktu yang dibutuhkan untuk mengkonsumsi 80% A!
· 0.0 (0)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



