Joko M
14 Agustus 2022 07:01
Iklan
Joko M
14 Agustus 2022 07:01
Pertanyaan
reaksi antara 250 ml larutan NH4OH 0,2 M dengan 250 ml larutan HCl 0,1 M, akan menghasilkan campuran dengan pH….(Kb NH4OH = 1 x 10-5)
1
1
Iklan
S. Zulaihah
Mahasiswa/Alumni Universitas Negeri Surabaya
03 Oktober 2022 14:48
<p>Jawaban yang benar adalah 9.</p><p> </p><p>Larutan asam atau basa lemah yang direaksikan dengan larutan asam atau basa kuat maka akan terjadi 2 kemungkinan.<br>1. Jika asam atau basa lemah bersisa maka akan terbentuk larutan penyangga.<br>2. Jika kedua pereaksi habis bereaksi maka akan terjadi hidrolisis parsial (sebagian).<br><br>▪︎menentukan mol masing-masing zat<br>mol NH4OH = M × V<br>mol NH4OH = 0,2 M × 250 ml<br>mol NH4OH = 50 mmol<br><br>mol HCl = M × V<br>mol HCl = 0,1 M × 250 ml<br>mol HCl = 25 mmol<br>Reaksi yang terjadi adalah seperti pada lampiran di bawah ini.<br>Dari perhitungan tersebut, mol NH4OH (basa lemah) bersisa sehingga larutan yang terbentuk merupakan larutan penyangga basa yang terdiri dari NH4OH (basa lemah) dan NH4Cl (garam dari basa lemah tersebut).</p><p>▪︎menentukan pH campuran</p><p>[OH⁻] = Kb × (mol basa / mol garam)</p><p>[OH⁻] = 10⁻⁵ × (25 mol / 25 mol)</p><p>[OH⁻] = 10⁻⁵ M</p><p>pOH = - log 10⁻⁵ </p><p>pOH = 5</p><p>pH = 14 - 5</p><p>pH = 9</p><p> </p><p>Jadi, pH campurannya adalah 9.</p>
Jawaban yang benar adalah 9.
Larutan asam atau basa lemah yang direaksikan dengan larutan asam atau basa kuat maka akan terjadi 2 kemungkinan.
1. Jika asam atau basa lemah bersisa maka akan terbentuk larutan penyangga.
2. Jika kedua pereaksi habis bereaksi maka akan terjadi hidrolisis parsial (sebagian).
▪︎menentukan mol masing-masing zat
mol NH4OH = M × V
mol NH4OH = 0,2 M × 250 ml
mol NH4OH = 50 mmol
mol HCl = M × V
mol HCl = 0,1 M × 250 ml
mol HCl = 25 mmol
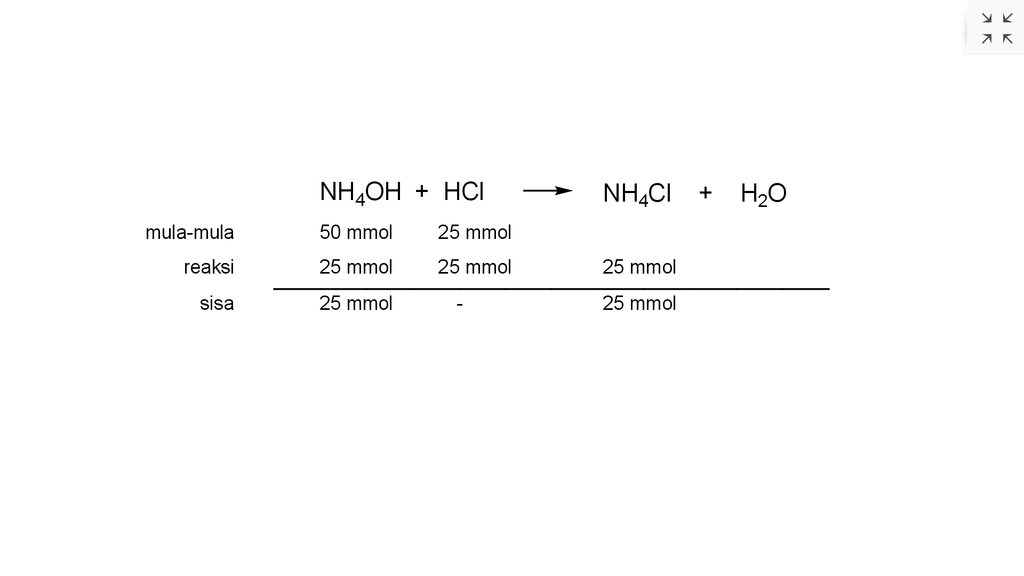
Reaksi yang terjadi adalah seperti pada lampiran di bawah ini.
Dari perhitungan tersebut, mol NH4OH (basa lemah) bersisa sehingga larutan yang terbentuk merupakan larutan penyangga basa yang terdiri dari NH4OH (basa lemah) dan NH4Cl (garam dari basa lemah tersebut).
▪︎menentukan pH campuran
[OH⁻] = Kb × (mol basa / mol garam)
[OH⁻] = 10⁻⁵ × (25 mol / 25 mol)
[OH⁻] = 10⁻⁵ M
pOH = - log 10⁻⁵
pOH = 5
pH = 14 - 5
pH = 9
Jadi, pH campurannya adalah 9.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke Forum
Biar Robosquad lain yang jawab soal kamu

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



