Sunshine F
08 Juni 2024 16:30
Iklan
Sunshine F
08 Juni 2024 16:30
Pertanyaan
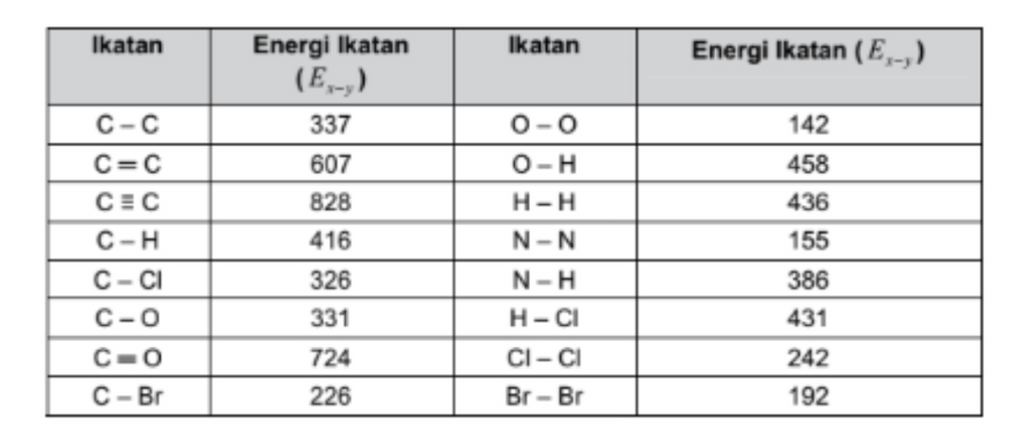
Perhatikan Tabel energi ikatan dibawah, tentukan nilai Delta H reaksi pada reaksi : H2(g) + Cl2(g) --> 2HCl(g) !
Perhatikan Tabel energi ikatan dibawah, tentukan nilai Delta H reaksi pada reaksi :
H2(g) + Cl2(g) --> 2HCl(g) !
1
1
Iklan
J. Siregar
09 Juni 2024 01:19
<p><strong>Jawaban yang benar adalah 44,4 kJ/mol.</strong></p><p> </p><p>Untuk menentukan ∆H reaksi, dapat juga menggunakan data dari energi yang diperlukan untuk memutuskan ikatan tersebut, sedangkan data energi yang diperlukan adalah reaksi kebalikan dari pemutusan ikatan.</p><p>Rumus menentukan perubahan entalpi (∆H) reaksi dari data energi ikatan diketahui:</p><p>∆H reaksi = ∑ energi pemutusan ikatan - ∑energi pembentukan ikatan</p><p> </p><p>Persamaan reaksi termokimia:</p><p>H ⎯ H + Cl ⎯ Cl → 2H ⎯ Cl</p><p>∆H reaksi = (energi ikatan H⎯H + energi ikatan Cl⎯Cl) - (2. energi ikatan H⎯Cl)</p><p>∆H reaksi = (436 + 242) - (2 × 431)</p><p>∆H reaksi = 678 - 862</p><p>∆H reaksi = -184 kJ/mol</p><p> </p><p><strong><u>Dengan demikian, besarnya ∆H reaksi tersebut adalah -184 kJ/mol.</u></strong></p>
Jawaban yang benar adalah 44,4 kJ/mol.
Untuk menentukan ∆H reaksi, dapat juga menggunakan data dari energi yang diperlukan untuk memutuskan ikatan tersebut, sedangkan data energi yang diperlukan adalah reaksi kebalikan dari pemutusan ikatan.
Rumus menentukan perubahan entalpi (∆H) reaksi dari data energi ikatan diketahui:
∆H reaksi = ∑ energi pemutusan ikatan - ∑energi pembentukan ikatan
Persamaan reaksi termokimia:
H ⎯ H + Cl ⎯ Cl → 2H ⎯ Cl
∆H reaksi = (energi ikatan H⎯H + energi ikatan Cl⎯Cl) - (2. energi ikatan H⎯Cl)
∆H reaksi = (436 + 242) - (2 × 431)
∆H reaksi = 678 - 862
∆H reaksi = -184 kJ/mol
Dengan demikian, besarnya ∆H reaksi tersebut adalah -184 kJ/mol.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



