Shesar V
28 Agustus 2022 14:57
Iklan
Shesar V
28 Agustus 2022 14:57
Pertanyaan
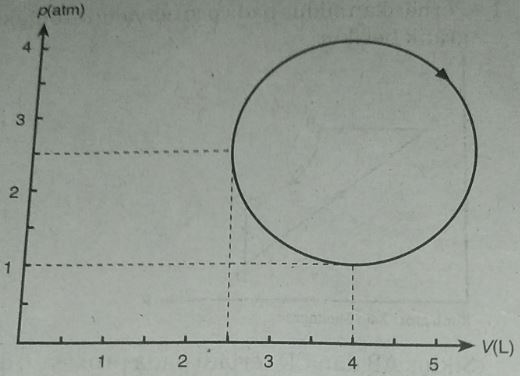
Perhatikan siklus pada sistem pemanasan gas yang ditunjukkan seperti gambar berikut! Pada grafik tersebut, sistem terjadi penurunan energi dalam sebesar 225 J. Jika sistem melakukan usaha, jumlah kalor pada sistem tersebut adalah .... (gunakan π = 3,14)
2
1
Iklan
Y. Frando
01 November 2022 22:08
<p>Jawaban yang benar adalah 481,5 J.</p><p> </p><p>Diketahui:</p><p>Grafik p-V termodinamika.</p><p>1 atm = 10^5 Pa</p><p>1 L = 10^-3 m^3</p><p>∆U = -225 J</p><p>π = 3,14</p><p> </p><p>Ditanya:</p><p>Kalor (Q) = ...?</p><p> </p><p>Jawab:</p><p>Konsep yang kita gunakan adalah usaha luar yang bekerja pada setiap proses keadaan gas. Dalam termodinamika terdapat 4 proses keadaan gas, yaitu isobarik, isokhorik, isotermik, dan adiabatik. Untuk satu sistem tertutup (siklus), besar usaha proses pada grafik diperoleh dengan menghitung luas yang berada di bawah grafik sesuai proses yang terjadi.</p><p>Selain itu, analisis hukum I Termodinamika dapat dituliskan sebagai:</p><p> </p><p>Q = W + ΔU,</p><p> </p><p>dengan:</p><p>Q = kalor (J)</p><p>W = usaha (J)</p><p>ΔU = perubahan energi dalam (J).</p><p> </p><p>Dari grafik pada soal, kita dapat memperoleh bentuk lingkaran, sehingga besar usaha dalam proses tersebut adalah luas lingkaran. Maka, hasil usaha diperoleh berikut ini.</p><p> </p><p>W = luas lingkaran</p><p>W = π x r1 x r2</p><p>W = π x (4 - 2,5) x 10^-3 x (2,5 - 1) x 10^5 </p><p>W = π x 1,5 x 1,5 x 10<sup>2</sup></p><p>W = 225π J.</p><p> </p><p>Sehingga, kalor yang diperoleh adalah:</p><p>Q = W + ΔU</p><p>Q = 225π + (-225)</p><p>Q = 225π - 225</p><p>Q = 225 (π - 1)</p><p>Q = 225 (3,14 - 1)</p><p>Q = 481,5 J.</p><p> </p><p>Jadi, jumlah kalor pada sistem tersebut adalah 481,5 J.</p>
Jawaban yang benar adalah 481,5 J.
Diketahui:
Grafik p-V termodinamika.
1 atm = 10^5 Pa
1 L = 10^-3 m^3
∆U = -225 J
π = 3,14
Ditanya:
Kalor (Q) = ...?
Jawab:
Konsep yang kita gunakan adalah usaha luar yang bekerja pada setiap proses keadaan gas. Dalam termodinamika terdapat 4 proses keadaan gas, yaitu isobarik, isokhorik, isotermik, dan adiabatik. Untuk satu sistem tertutup (siklus), besar usaha proses pada grafik diperoleh dengan menghitung luas yang berada di bawah grafik sesuai proses yang terjadi.
Selain itu, analisis hukum I Termodinamika dapat dituliskan sebagai:
Q = W + ΔU,
dengan:
Q = kalor (J)
W = usaha (J)
ΔU = perubahan energi dalam (J).
Dari grafik pada soal, kita dapat memperoleh bentuk lingkaran, sehingga besar usaha dalam proses tersebut adalah luas lingkaran. Maka, hasil usaha diperoleh berikut ini.
W = luas lingkaran
W = π x r1 x r2
W = π x (4 - 2,5) x 10^-3 x (2,5 - 1) x 10^5
W = π x 1,5 x 1,5 x 102
W = 225π J.
Sehingga, kalor yang diperoleh adalah:
Q = W + ΔU
Q = 225π + (-225)
Q = 225π - 225
Q = 225 (π - 1)
Q = 225 (3,14 - 1)
Q = 481,5 J.
Jadi, jumlah kalor pada sistem tersebut adalah 481,5 J.
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



