Made K
12 Oktober 2023 15:52
Iklan
Made K
12 Oktober 2023 15:52
Pertanyaan
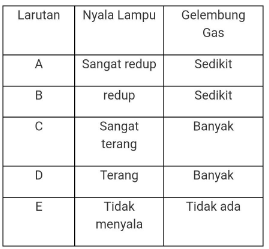
perhatikan hasil percobaan daya hantar listrik larutan di bawah ini! Urutkan larutan tersebut berdasarkan kenaikan daya hantar listrik!
1
1
Iklan
I. Qatrunnada
Mahasiswa/Alumni Univesitas Islam Indonesia
30 Oktober 2023 08:25
<p>Jawab : Berdasarkan kenaikan daya listrik dari terlemah hingga terkuat adalah E - A - B - D - C</p><p> </p><p>Berdasarkan daya hantar listrik, larutan dibedakan menjadi larutan elektrolit kuat, larutan elektrolit lemah dan nonelektrolit.</p><p> </p><p><strong>Senyawa elektrolit kuat apabila dilarutkan dalam air akan menghasilkan larutan elektrolit kuat.</strong></p><ul><li>Larutan elektrolit kuat saat diuji dengan alat penguji elektrolit menghasilkan nyala lampu terang dan banyak menghasilkan gelembung-gelembung gas di sekitar elektroda.</li><li>Larutan elektrolit dapat menghantarkan arus listrik karena terdapat ion-ion yang bergerak bebas dalam lautannya yang dapat menghantarkan arus listrik. </li><li>Contoh senyawa yang dapat membentuk elektrolit kuat adalah asam kuat, basa kuat dan garam. </li></ul><p> </p><p><strong>Senyawa elektrolit lemah apabila dilarutkan dalam air akan menghasilkan larutan elektrolit lemah.</strong></p><ul><li>Larutan elektrolit lemah saat diuji dengan alat penguji elektrolit menghasilkan nyala lampu redup dan sedikit gelembung-gelembung gas di sekitar elektroda. Selain itu hasil percobaan juga bisa memberikan hasil lampu tidak menyala dan terdapat gelembung-gelembung gas di sekitar elektroda.</li><li>Larutan elektrolit dapat menghantarkan arus listrik karena terdapat ion-ion yang bergerak bebas dalam larutannya yang dapat menghantarkan arus listrik.</li><li>Contoh senyawa yang dapat membentuk elektrolit lemah adalah asam lemah, basa lemah. <br> </li></ul><p><strong>Senyawa non-elektrolit apabila dilarutkan dalam air akan menghasilkan larutan non-elektrolit.</strong></p><ul><li>Larutan non-elektrolit saat diuji dengan alat penguji elektrolit tidak dapat menyalakan lampu dan tidak menghasilkan gelembung-gelembung gas di sekitar elektroda.</li><li>Larutan non-elektrolit tidak dapat menghantarkan arus listrik karena tidak terdapat ion-ion yang bergerak bebas dalam larutannya yang dapat menghantarkan arus listrik.</li><li>Contoh senyawa yang dapat membentuk non-elektrolit adalah larutan senyawa organik seperti glukosa, urea, formaldehid. </li></ul><p> </p><p>Larutan E : non elektrolit</p><p>Larutan A : elektrolit lemah</p><p>Larutan B : elektrolit lemah</p><p>Larutan D : elektrolit kuat</p><p>Larutan C : elektrolit kuat </p><p> </p><p>Berdasarkan kenaikan daya listrik dari terlemah hingga terkuat adalah E - A - B - D - C</p>
Jawab : Berdasarkan kenaikan daya listrik dari terlemah hingga terkuat adalah E - A - B - D - C
Berdasarkan daya hantar listrik, larutan dibedakan menjadi larutan elektrolit kuat, larutan elektrolit lemah dan nonelektrolit.
Senyawa elektrolit kuat apabila dilarutkan dalam air akan menghasilkan larutan elektrolit kuat.
- Larutan elektrolit kuat saat diuji dengan alat penguji elektrolit menghasilkan nyala lampu terang dan banyak menghasilkan gelembung-gelembung gas di sekitar elektroda.
- Larutan elektrolit dapat menghantarkan arus listrik karena terdapat ion-ion yang bergerak bebas dalam lautannya yang dapat menghantarkan arus listrik.
- Contoh senyawa yang dapat membentuk elektrolit kuat adalah asam kuat, basa kuat dan garam.
Senyawa elektrolit lemah apabila dilarutkan dalam air akan menghasilkan larutan elektrolit lemah.
- Larutan elektrolit lemah saat diuji dengan alat penguji elektrolit menghasilkan nyala lampu redup dan sedikit gelembung-gelembung gas di sekitar elektroda. Selain itu hasil percobaan juga bisa memberikan hasil lampu tidak menyala dan terdapat gelembung-gelembung gas di sekitar elektroda.
- Larutan elektrolit dapat menghantarkan arus listrik karena terdapat ion-ion yang bergerak bebas dalam larutannya yang dapat menghantarkan arus listrik.
- Contoh senyawa yang dapat membentuk elektrolit lemah adalah asam lemah, basa lemah.
Senyawa non-elektrolit apabila dilarutkan dalam air akan menghasilkan larutan non-elektrolit.
- Larutan non-elektrolit saat diuji dengan alat penguji elektrolit tidak dapat menyalakan lampu dan tidak menghasilkan gelembung-gelembung gas di sekitar elektroda.
- Larutan non-elektrolit tidak dapat menghantarkan arus listrik karena tidak terdapat ion-ion yang bergerak bebas dalam larutannya yang dapat menghantarkan arus listrik.
- Contoh senyawa yang dapat membentuk non-elektrolit adalah larutan senyawa organik seperti glukosa, urea, formaldehid.
Larutan E : non elektrolit
Larutan A : elektrolit lemah
Larutan B : elektrolit lemah
Larutan D : elektrolit kuat
Larutan C : elektrolit kuat
Berdasarkan kenaikan daya listrik dari terlemah hingga terkuat adalah E - A - B - D - C
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



