Sunshine F
09 Juni 2024 04:42
Iklan
Sunshine F
09 Juni 2024 04:42
Pertanyaan
Pada reaksi A + B → C diperoleh data : Persamaan laju reaksinya adalah…
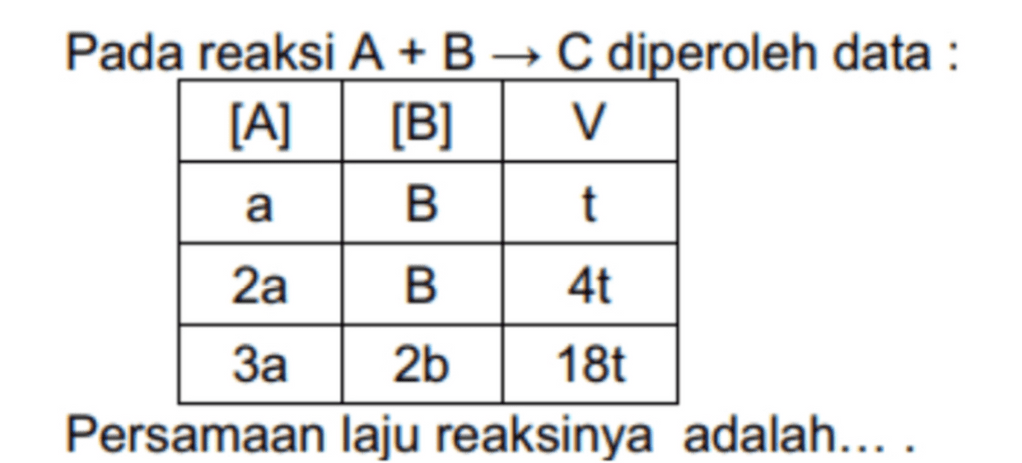
Pada reaksi A + B → C diperoleh data :
Persamaan laju reaksinya adalah…
1
1
Iklan
J. Siregar
09 Juni 2024 06:12
<p><strong>Jawaban yang benar adalah v = k [A]² [B].</strong></p><p> </p><p><strong>Orde reaksi</strong> merupakan bilangan eksponen yang menyatakan hubungan antara laju reaksi kimia dan konsentrasi reaktan yang terlibat di dalamnya. Untuk memperoleh <strong>orde reaksi maka kita bentuk </strong>persamaan laju umum sehingga hukum laju terpenuhi.</p><p>Perlu diingat juga bahwa orde reaksi hanya ditentukan dari data percobaan.</p><p> </p><p>Persamaan laju: v = k [A]<sup>m</sup> [B]<sup>n</sup></p><p>v = laju reaksi (M/s)</p><p>k = tetapan laju (bergantung orde reaksi)</p><p>m = orde reaksi A</p><p>n = orde reaksi B</p><p>Penentuan setiap orde kita bandingkan laju dan konsentrasinya, nilai k dan konsentrasi zat yang tetap dapat diabaikan.</p><ul><li>Orde A ditentukan dari data percobaan B yang konstan yaitu data 1 dan 2.</li></ul><p>v<sub>2</sub>/v<sub>1</sub> = ([A]<sub>2</sub>/[A]<sub>1</sub>)<sup>m</sup></p><p>4t/t = (2a/a)<sup>m</sup></p><p>4 = 2<sup>m</sup></p><p>2<sup>2</sup> = 2<sup>m</sup></p><p>m = 2</p><ul><li>Orde B ditentukan dari data percobaan A yang konstan, tetapi tidak ada data yang konstan sehingga nilai m kita substitusi untuk mencari orde B, misal percobaan 1 dan 2.</li></ul><p>v<sub>3</sub>/v<sub>2</sub> = ([A]<sub>3</sub>/[A]<sub>2</sub>)<sup>m </sup>([B]<sub>3</sub>/[B]<sub>2</sub>)<sup>n</sup></p><p>18t/4t = (3a/2a)²<sup> </sup>(2b/b)<sup>b</sup></p><p>9/2 = (9/4) 2<sup>b</sup></p><p>9/2 x 4/9 = 2<sup>b</sup></p><p>2 = 2<sup>b</sup></p><p>b = 1</p><p> </p><p> </p><p>Menentukan persamaan laju</p><p>Berdasarkan perhitungan di atas, orde A<sub> </sub>= 2 dan B = 1 maka persamaan lajunya adalah: v = k [A]²[B]</p><p> </p><p>Jadi, persamaan laju reaksi adalah v = k [A] [B].</p>
Jawaban yang benar adalah v = k [A]² [B].
Orde reaksi merupakan bilangan eksponen yang menyatakan hubungan antara laju reaksi kimia dan konsentrasi reaktan yang terlibat di dalamnya. Untuk memperoleh orde reaksi maka kita bentuk persamaan laju umum sehingga hukum laju terpenuhi.
Perlu diingat juga bahwa orde reaksi hanya ditentukan dari data percobaan.
Persamaan laju: v = k [A]m [B]n
v = laju reaksi (M/s)
k = tetapan laju (bergantung orde reaksi)
m = orde reaksi A
n = orde reaksi B
Penentuan setiap orde kita bandingkan laju dan konsentrasinya, nilai k dan konsentrasi zat yang tetap dapat diabaikan.
- Orde A ditentukan dari data percobaan B yang konstan yaitu data 1 dan 2.
v2/v1 = ([A]2/[A]1)m
4t/t = (2a/a)m
4 = 2m
22 = 2m
m = 2
- Orde B ditentukan dari data percobaan A yang konstan, tetapi tidak ada data yang konstan sehingga nilai m kita substitusi untuk mencari orde B, misal percobaan 1 dan 2.
v3/v2 = ([A]3/[A]2)m ([B]3/[B]2)n
18t/4t = (3a/2a)² (2b/b)b
9/2 = (9/4) 2b
9/2 x 4/9 = 2b
2 = 2b
b = 1
Menentukan persamaan laju
Berdasarkan perhitungan di atas, orde A = 2 dan B = 1 maka persamaan lajunya adalah: v = k [A]²[B]
Jadi, persamaan laju reaksi adalah v = k [A] [B].
· 0.0 (0)
Iklan
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke AiRIS
Yuk, cobain chat dan belajar bareng AiRIS, teman pintarmu!

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



