Bila B

03 September 2024 10:59
Iklan
Bila B

03 September 2024 10:59
Pertanyaan
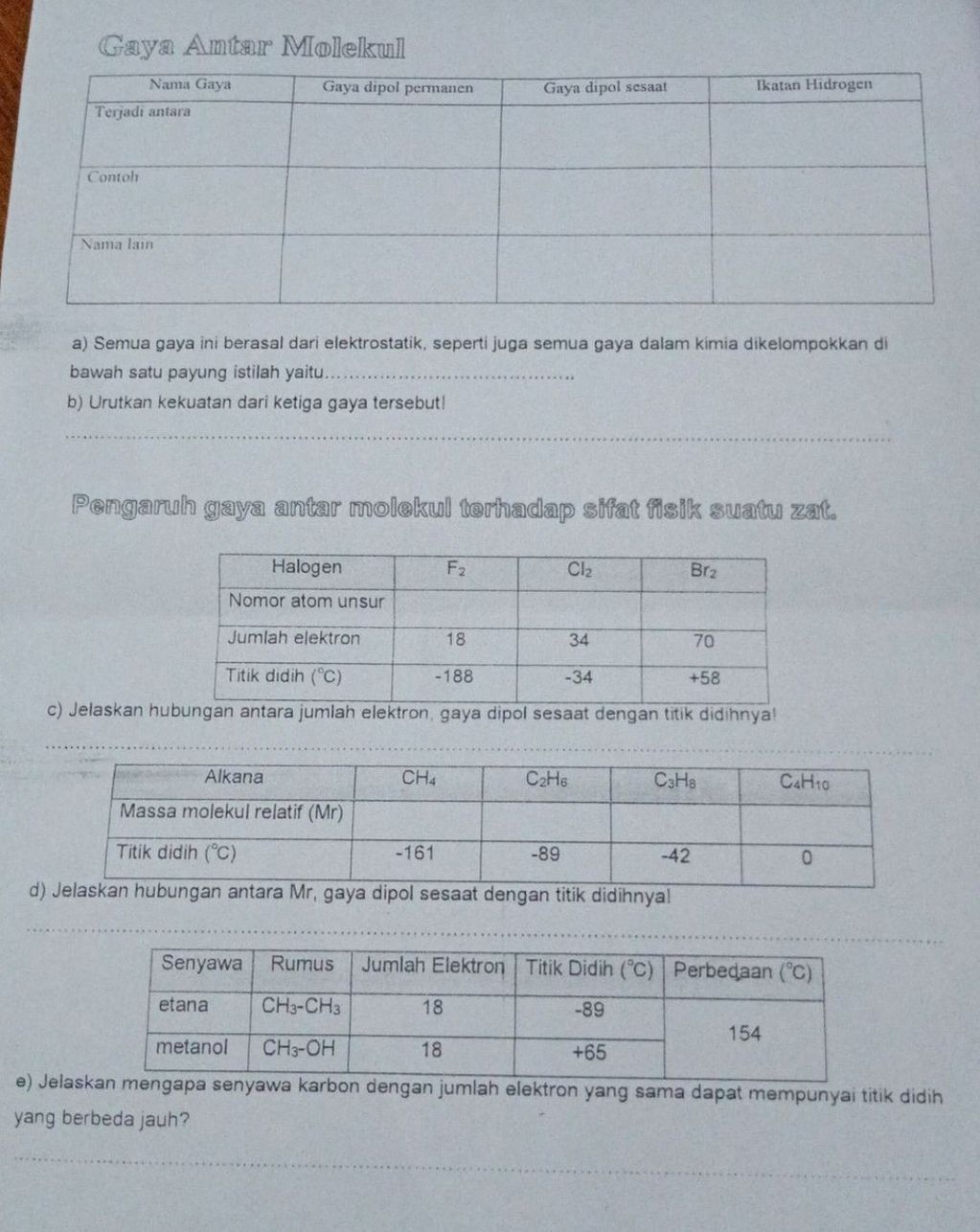
Helppp ini bagian b, c, d, dan e
Helppp ini bagian b, c, d, dan e
5
2
Iklan
Tyrannosaurus T
03 September 2024 11:38
<p><strong>c. Hubungan Antara Jumlah Elektron, Gaya Dipol Sesaat, dan Titik Didih pada Halogen (F₂, Cl₂, Br₂)</strong></p><p><strong>Penjelasan:</strong></p><p><strong>Jumlah Elektron:</strong> Fluorin (F₂), klorin (Cl₂), dan bromin (Br₂) semuanya adalah molekul diatomik yang termasuk dalam golongan halogen di tabel periodik. Nomor atomnya menunjukkan jumlah total elektron di setiap atom (9 untuk F, 17 untuk Cl, dan 35 untuk Br), tetapi untuk molekul diatomik, kita menjumlahkan elektron dari dua atom:</p><ul><li><strong>F₂:</strong> Jumlah elektron = 2 x 9 = 18</li><li><strong>Cl₂:</strong> Jumlah elektron = 2 x 17 = 34</li><li><strong>Br₂:</strong> Jumlah elektron = 2 x 35 = 70</li></ul><p><strong>Gaya Dipol Sesaat (London Dispersion Forces):</strong> Gaya dispersi London adalah gaya tarik menarik lemah yang dihasilkan dari fluktuasi sementara dalam distribusi elektron yang menciptakan dipol sesaat dalam molekul nonpolar. Besarnya gaya ini bergantung pada jumlah elektron dalam molekul; semakin banyak elektron, semakin kuat gaya London.</p><p><strong>Titik Didih:</strong></p><ul><li><strong>F₂:</strong> -188°C</li><li><strong>Cl₂:</strong> -34°C</li><li><strong>Br₂:</strong> +58°C</li></ul><p><strong>Hubungan:</strong></p><ol><li><strong>Jumlah Elektron dan Gaya Dipol Sesaat:</strong><ul><li>Seiring bertambahnya jumlah elektron (dari F₂ ke Br₂), gaya dispersi London meningkat karena awan elektron menjadi lebih besar dan lebih mudah berubah bentuk, menciptakan dipol sesaat yang lebih kuat.</li></ul></li><li><strong>Gaya Dipol Sesaat dan Titik Didih:</strong><ul><li>Semakin kuat gaya dipol sesaat (dispersi London), semakin tinggi titik didihnya karena diperlukan lebih banyak energi untuk memutuskan interaksi antarmolekul ini.</li></ul></li><li><strong>Contoh:</strong><ul><li>F₂ memiliki jumlah elektron paling sedikit dan gaya dispersi London paling lemah, sehingga titik didihnya sangat rendah (-188°C).</li><li>Br₂ memiliki jumlah elektron paling banyak dan gaya dispersi London paling kuat, sehingga titik didihnya lebih tinggi (+58°C).</li></ul></li></ol><p> </p><p><strong>d. Hubungan Antara Massa Molekul Relatif (Mr), Gaya Dipol Sesaat, dan Titik Didih pada Alkan (CH₄, C₂H₆, C₃H₈, C₄H₁₀)</strong></p><p><strong>Penjelasan:</strong></p><p><strong>Massa Molekul Relatif (Mr):</strong> Ini mengacu pada massa total molekul berdasarkan massa atom relatif dari atom-atom penyusunnya. Dalam deret alkana (CH₄, C₂H₆, C₃H₈, C₄H₁₀), Mr bertambah seiring dengan bertambahnya jumlah atom karbon dan hidrogen.</p><ul><li><strong>CH₄ (Metana):</strong> Mr ≈ 16, Titik Didih: -161°C</li><li><strong>C₂H₆ (Etana):</strong> Mr ≈ 30, Titik Didih: -89°C</li><li><strong>C₃H₈ (Propana):</strong> Mr ≈ 44, Titik Didih: -42°C</li><li><strong>C₄H₁₀ (Butana):</strong> Mr ≈ 58, Titik Didih: 0°C</li></ul><p><strong>Gaya Dipol Sesaat (London Dispersion Forces):</strong> Sama seperti halogen, alkana adalah molekul nonpolar sehingga gaya antarmolekul utama yang mempengaruhi titik didih adalah gaya dispersi London.</p><p><strong>Hubungan:</strong></p><p><strong>Massa Molekul Relatif (Mr) dan Gaya Dipol Sesaat:</strong></p><ul><li>Seiring bertambahnya massa molekul relatif (Mr), jumlah elektron juga bertambah, menyebabkan awan elektron menjadi lebih besar dan lebih mudah berubah bentuk.</li><li>Hal ini meningkatkan gaya dispersi London, sehingga gaya tarik menarik antar molekul menjadi lebih kuat.</li></ul><p><strong>Gaya Dipol Sesaat dan Titik Didih:</strong></p><ul><li>Semakin kuat gaya dispersi London, semakin banyak energi yang dibutuhkan untuk memisahkan molekul-molekul ini, yang meningkatkan titik didih.</li></ul><p><strong>Contoh:</strong></p><ul><li>CH₄ (metana) dengan Mr terendah memiliki gaya dispersi London yang lemah, sehingga titik didihnya sangat rendah (-161°C).</li><li>C₄H₁₀ (butana) dengan Mr tertinggi memiliki gaya dispersi London yang lebih kuat, sehingga titik didihnya lebih tinggi (0°C).</li></ul><p> </p><p><strong>e. Perbedaan Titik Didih Antara Etana (CH₃-CH₃) dan Metanol (CH₃-OH) Meski Jumlah Elektron Sama</strong></p><p><strong>Penjelasan:</strong></p><p><strong>Jumlah Elektron Sama:</strong></p><ul><li>Etana (CH₃-CH₃) dan metanol (CH₃-OH) keduanya memiliki jumlah total elektron yang sama (18 elektron).</li></ul><p><strong>Perbedaan Titik Didih:</strong></p><ul><li><strong>Etana (CH₃-CH₃):</strong> Titik didih -89°C</li><li><strong>Metanol (CH₃-OH):</strong> Titik didih +65°C</li></ul><p><strong>Penyebab Utama Perbedaan:</strong></p><p><strong>Interaksi Antarmolekul:</strong></p><ul><li><strong>Etana (CH₃-CH₃):</strong> Merupakan molekul nonpolar, sehingga hanya memiliki gaya dispersi London yang relatif lemah sebagai gaya antarmolekul utama.</li><li><strong>Metanol (CH₃-OH):</strong> Mengandung gugus hidroksil (-OH), yang dapat membentuk ikatan hidrogen. Ikatan hidrogen adalah gaya antarmolekul yang jauh lebih kuat dibandingkan dengan gaya dispersi London.</li></ul><p><strong>Ikatan Hidrogen:</strong></p><ul><li>Ikatan hidrogen di metanol menciptakan gaya tarik menarik yang sangat kuat antar molekul, yang membutuhkan energi lebih besar untuk memutuskan dan mengubah fase cair ke gas.</li><li>Akibatnya, titik didih metanol jauh lebih tinggi (+65°C) dibandingkan dengan etana (-89°C), meskipun jumlah elektron keduanya sama.</li></ul><p><strong>Kesimpulan:</strong></p><p>Perbedaan dalam titik didih meskipun jumlah elektron yang sama disebabkan oleh perbedaan jenis dan kekuatan gaya antarmolekul. Molekul yang dapat membentuk ikatan hidrogen (seperti metanol) memiliki titik didih yang lebih tinggi dibandingkan dengan molekul nonpolar (seperti etana) karena ikatan hidrogen lebih kuat daripada gaya dispersi London.</p><p> </p>
c. Hubungan Antara Jumlah Elektron, Gaya Dipol Sesaat, dan Titik Didih pada Halogen (F₂, Cl₂, Br₂)
Penjelasan:
Jumlah Elektron: Fluorin (F₂), klorin (Cl₂), dan bromin (Br₂) semuanya adalah molekul diatomik yang termasuk dalam golongan halogen di tabel periodik. Nomor atomnya menunjukkan jumlah total elektron di setiap atom (9 untuk F, 17 untuk Cl, dan 35 untuk Br), tetapi untuk molekul diatomik, kita menjumlahkan elektron dari dua atom:
- F₂: Jumlah elektron = 2 x 9 = 18
- Cl₂: Jumlah elektron = 2 x 17 = 34
- Br₂: Jumlah elektron = 2 x 35 = 70
Gaya Dipol Sesaat (London Dispersion Forces): Gaya dispersi London adalah gaya tarik menarik lemah yang dihasilkan dari fluktuasi sementara dalam distribusi elektron yang menciptakan dipol sesaat dalam molekul nonpolar. Besarnya gaya ini bergantung pada jumlah elektron dalam molekul; semakin banyak elektron, semakin kuat gaya London.
Titik Didih:
- F₂: -188°C
- Cl₂: -34°C
- Br₂: +58°C
Hubungan:
- Jumlah Elektron dan Gaya Dipol Sesaat:
- Seiring bertambahnya jumlah elektron (dari F₂ ke Br₂), gaya dispersi London meningkat karena awan elektron menjadi lebih besar dan lebih mudah berubah bentuk, menciptakan dipol sesaat yang lebih kuat.
- Gaya Dipol Sesaat dan Titik Didih:
- Semakin kuat gaya dipol sesaat (dispersi London), semakin tinggi titik didihnya karena diperlukan lebih banyak energi untuk memutuskan interaksi antarmolekul ini.
- Contoh:
- F₂ memiliki jumlah elektron paling sedikit dan gaya dispersi London paling lemah, sehingga titik didihnya sangat rendah (-188°C).
- Br₂ memiliki jumlah elektron paling banyak dan gaya dispersi London paling kuat, sehingga titik didihnya lebih tinggi (+58°C).
d. Hubungan Antara Massa Molekul Relatif (Mr), Gaya Dipol Sesaat, dan Titik Didih pada Alkan (CH₄, C₂H₆, C₃H₈, C₄H₁₀)
Penjelasan:
Massa Molekul Relatif (Mr): Ini mengacu pada massa total molekul berdasarkan massa atom relatif dari atom-atom penyusunnya. Dalam deret alkana (CH₄, C₂H₆, C₃H₈, C₄H₁₀), Mr bertambah seiring dengan bertambahnya jumlah atom karbon dan hidrogen.
- CH₄ (Metana): Mr ≈ 16, Titik Didih: -161°C
- C₂H₆ (Etana): Mr ≈ 30, Titik Didih: -89°C
- C₃H₈ (Propana): Mr ≈ 44, Titik Didih: -42°C
- C₄H₁₀ (Butana): Mr ≈ 58, Titik Didih: 0°C
Gaya Dipol Sesaat (London Dispersion Forces): Sama seperti halogen, alkana adalah molekul nonpolar sehingga gaya antarmolekul utama yang mempengaruhi titik didih adalah gaya dispersi London.
Hubungan:
Massa Molekul Relatif (Mr) dan Gaya Dipol Sesaat:
- Seiring bertambahnya massa molekul relatif (Mr), jumlah elektron juga bertambah, menyebabkan awan elektron menjadi lebih besar dan lebih mudah berubah bentuk.
- Hal ini meningkatkan gaya dispersi London, sehingga gaya tarik menarik antar molekul menjadi lebih kuat.
Gaya Dipol Sesaat dan Titik Didih:
- Semakin kuat gaya dispersi London, semakin banyak energi yang dibutuhkan untuk memisahkan molekul-molekul ini, yang meningkatkan titik didih.
Contoh:
- CH₄ (metana) dengan Mr terendah memiliki gaya dispersi London yang lemah, sehingga titik didihnya sangat rendah (-161°C).
- C₄H₁₀ (butana) dengan Mr tertinggi memiliki gaya dispersi London yang lebih kuat, sehingga titik didihnya lebih tinggi (0°C).
e. Perbedaan Titik Didih Antara Etana (CH₃-CH₃) dan Metanol (CH₃-OH) Meski Jumlah Elektron Sama
Penjelasan:
Jumlah Elektron Sama:
- Etana (CH₃-CH₃) dan metanol (CH₃-OH) keduanya memiliki jumlah total elektron yang sama (18 elektron).
Perbedaan Titik Didih:
- Etana (CH₃-CH₃): Titik didih -89°C
- Metanol (CH₃-OH): Titik didih +65°C
Penyebab Utama Perbedaan:
Interaksi Antarmolekul:
- Etana (CH₃-CH₃): Merupakan molekul nonpolar, sehingga hanya memiliki gaya dispersi London yang relatif lemah sebagai gaya antarmolekul utama.
- Metanol (CH₃-OH): Mengandung gugus hidroksil (-OH), yang dapat membentuk ikatan hidrogen. Ikatan hidrogen adalah gaya antarmolekul yang jauh lebih kuat dibandingkan dengan gaya dispersi London.
Ikatan Hidrogen:
- Ikatan hidrogen di metanol menciptakan gaya tarik menarik yang sangat kuat antar molekul, yang membutuhkan energi lebih besar untuk memutuskan dan mengubah fase cair ke gas.
- Akibatnya, titik didih metanol jauh lebih tinggi (+65°C) dibandingkan dengan etana (-89°C), meskipun jumlah elektron keduanya sama.
Kesimpulan:
Perbedaan dalam titik didih meskipun jumlah elektron yang sama disebabkan oleh perbedaan jenis dan kekuatan gaya antarmolekul. Molekul yang dapat membentuk ikatan hidrogen (seperti metanol) memiliki titik didih yang lebih tinggi dibandingkan dengan molekul nonpolar (seperti etana) karena ikatan hidrogen lebih kuat daripada gaya dispersi London.
· 0.0 (0)
Iklan
J. Siregar
04 September 2024 09:45
Jawaban yang benar adalah memiliki jumlah elektron paling banyak dan gaya dispersi London paling kuat, sehingga titik didihnya lebih tinggi. Jumlah Elektron: Fluorin (F₂), klorin (Cl₂), dan bromin (Br₂) semuanya adalah molekul diatomik yang termasuk dalam golongan halogen di tabel periodik. Nomor atomnya menunjukkan jumlah total elektron di setiap atom (9 untuk F, 17 untuk Cl, dan 35 untuk Br), tetapi untuk molekul diatomik, kita menjumlahkan elektron dari dua atom: F₂: Jumlah elektron = 2 x 9 = 18 Cl₂: Jumlah elektron = 2 x 17 = 34 Br₂: Jumlah elektron = 2 x 35 = 70 Gaya Dipol Sesaat (London Dispersion Forces): Gaya dispersi London adalah gaya tarik menarik lemah yang dihasilkan dari fluktuasi sementara dalam distribusi elektron yang menciptakan dipol sesaat dalam molekul nonpolar. Besarnya gaya ini bergantung pada jumlah elektron dalam molekul; semakin banyak elektron, semakin kuat gaya London. Titik Didih: F₂: -188°C Cl₂: -34°C Br₂: 58°C Hubungan: Jumlah Elektron dan Gaya Dipol Sesaat: Seiring bertambahnya jumlah elektron (dari F₂ ke Br₂), gaya dispersi London meningkat karena awan elektron menjadi lebih besar dan lebih mudah berubah bentuk, menciptakan dipol sesaat yang lebih kuat. Gaya Dipol Sesaat dan Titik Didih: Semakin kuat gaya dipol sesaat (dispersi London), semakin tinggi titik didihnya karena diperlukan lebih banyak energi untuk memutuskan interaksi antarmolekul ini. Contoh: F₂ memiliki jumlah elektron paling sedikit dan gaya dispersi London paling lemah, sehingga titik didihnya sangat rendah (-188°C). Br₂ memiliki jumlah elektron paling banyak dan gaya dispersi London paling kuat, sehingga titik didihnya lebih tinggi (58°C). Jadi, jawaban yang benar adalah memiliki jumlah elektron paling banyak dan gaya dispersi London paling kuat, sehingga titik didihnya lebih tinggi.
· 0.0 (0)
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke Forum
Biar Robosquad lain yang jawab soal kamu

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!



