Salah satu konsep dari reaksi redoks adalah perubahan bilangan oksidasi. Pengertian reaksi redoks berdasarkan perubahan biloks adalah sebagai berikut:
- Reduksi merupakan reaksi karena adanya penurunan bilangan oksidasi.
- Oksidasi merupakan reaksi karena adanya peningkatan bilangan oksidasi.
Selain itu pada reaksi redoks terdapat istilah yang disebut dengan reduktor dan oksidator.
- Reduktor merupakan zat yang mengalami oksidasi.
- Oksidator merupakan zat yang mengalami reduksi.

Unsur O: bilangan oksidasi O sebesar -2, kecuali pada peroksida, superoksida, dan unsur bebas. Tidak ada peroksida, superoksida, dan unsur bebas, berarti atom O tidak mengalami perubahan bilangan oksidasi.
Unsur Fe: ada di  dan unsur bebas Fe.
dan unsur bebas Fe.
 :
:

Sebagai unsur bebas, bilangan oksidasi Fe sebesar 0. Dengan demikian, Fe mengalami penurunan bilangan oksidasi dari +3 ke 0 (reduksi) sehingga  merupakan oksidator.
merupakan oksidator.
Unsur C: ada di  dan
dan  .
.


 .
.

Dengan demikian, C mengalami kenaikan bilangan oksidasi dari +2 ke +4 (oksidasi) sehingga  merupakan reduktor.
merupakan reduktor.

Unsur O: bilangan oksidasi O sebesar -2, kecuali pada peroksida, superoksida, dan unsur bebas. Tidak ada peroksida, superoksida, dan unsur bebas, berarti atom O tidak mengalami perubahan bilangan oksidasi.
Unsur Cr: ada di  dan unsur bebas Cr.
dan unsur bebas Cr.
 :
:

Sebagai unsur bebas, bilangan oksidasi Cr sebesar 0. Dengan demikian, Cr mengalami penurunan bilangan oksidasi dari +3 ke 0 (reduksi) sehingga  merupakan oksidator.
merupakan oksidator.
Unsur Al: ada di unsur bebas Al dan  .
.
Sebagai unsur bebas, bilangan oksidasi Al sebesar 0.
 :
:

Dengan demikian, Al mengalami kenaikan bilangan oksidasi dari 0 ke +3 (oksidasi) sehingga Al merupakan reduktor.

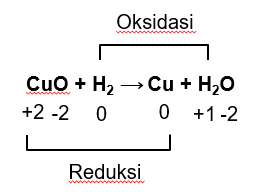
Unsur O: bilangan oksidasi O sebesar -2, kecuali pada peroksida, superoksida, dan unsur bebas. Tidak ada peroksida, superoksida, dan unsur bebas, berarti atom O tidak mengalami perubahan bilangan oksidasi.
Unsur Cu: ada di  dan unsur bebas Cu.
dan unsur bebas Cu.
 :
:

Sebagai unsur bebas, bilangan oksidasi Cu sebesar 0. Dengan demikian, Cu mengalami penurunan bilangan oksidasi dari +2 ke 0 (reduksi) sehingga  merupakan oksidator.
merupakan oksidator.
Unsur H: bilangan oksidasi unsur H sebesar +1 kecuali pada hidrida dan unsur bebas. Pada reaksi, ada unsur bebas H. Dengan demikian, H mengalami kenaikan bilangan oksidasi dari 0 ke +1 (oksidasi) sehingga  sebagai reduktor.
sebagai reduktor.
Jadi, kesimpulan jawaban untuk soal tersebut adalah:
a. Oksidatornya adalah  dan reduktornya adalah
dan reduktornya adalah 
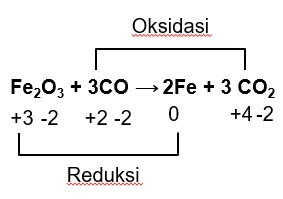
b. Oksidatornya adalah  dan reduktornya adalah Al.
dan reduktornya adalah Al.
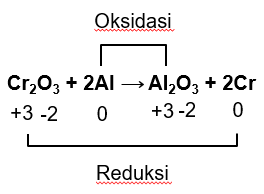
c. Oksidatornya adalah  dan reduktornya adalah
dan reduktornya adalah