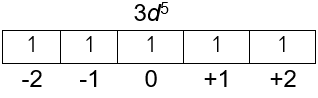Iklan
Iklan
Pertanyaan
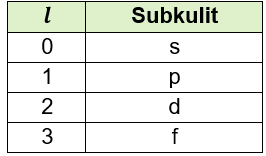
Setiap elektron memiliki 4 bilangan kuantum, yaitu bilangan kuantum utama, bilangan kuantum azimuth, bilangan kuantum magnetik, dan bilangan kuantum spin. Tentukan konfigurasi elektron dari unsur berikut ini dan tentukan bilangan kuantum elektron terakhir pada atom: a. 24 Cr
Setiap elektron memiliki 4 bilangan kuantum, yaitu bilangan kuantum utama, bilangan kuantum azimuth, bilangan kuantum magnetik, dan bilangan kuantum spin.
Tentukan konfigurasi elektron dari unsur berikut ini dan tentukan bilangan kuantum elektron terakhir pada atom:
a.
Iklan
IY
I. Yassa
Master Teacher
Jawaban terverifikasi
8
5.0 (1 rating)
SA
Siti Aziza
sangat membantu saya dalam semua mata pelajaran 😊👍👍👍👍👍👍👍👍👍👍👍👍👍👍👍👍👍👍
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia