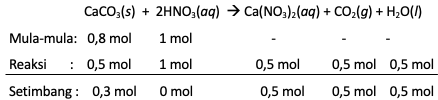Iklan
Iklan
Pertanyaan
Senyawa HNO 3 dengan massa 63 gram direaksikan dengan 80 gram CaCO 3 . Dengan persamaan reaksi sebagai berikut, CaCO 3 ( s ) + HNO 3 ( a q ) → Ca ( NO 3 ) 2 ( a q ) + CO 2 ( g ) + H 2 O ( l ) Tentukan, a. Pereaksi pembatas b. Jumlah mol dari pereaksi berlebih c. Volume gas CO 2 pada keadaan STP
Senyawa dengan massa 63 gram direaksikan dengan 80 gram . Dengan persamaan reaksi sebagai berikut,
Tentukan,
a. Pereaksi pembatas
b. Jumlah mol dari pereaksi berlebih
c. Volume gas pada keadaan STP
Iklan
PC
P. Cucu
Master Teacher
Mahasiswa/Alumni Universitas Negeri Jakarta
Jawaban terverifikasi
2
0.0 (0 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia