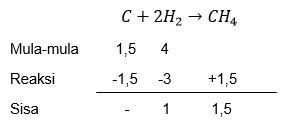Iklan
Iklan
Pertanyaan
Perbandingan massa karbon (C) terhadap hidrogen (H) dalam senyawa metana ( CH 4 ) adalah 3 : 1. Sebanyak 18 gram karbon direaksikan dengan 8 gram hidrogen. a. Apakah semua zat akan habis bereaksi? Jika ada yang habis zat manakah itu? b. Berapa gram sisa zat saat akhir? c. Berapa gram metana yang dapat dihasilkan?
Perbandingan massa karbon (C) terhadap hidrogen (H) dalam senyawa metana adalah 3 : 1. Sebanyak 18 gram karbon direaksikan dengan 8 gram hidrogen.
a. Apakah semua zat akan habis bereaksi? Jika ada yang habis zat manakah itu?
b. Berapa gram sisa zat saat akhir?
c. Berapa gram metana yang dapat dihasilkan?
Iklan
DZ
D. Zharva
Master Teacher
Jawaban terverifikasi
16
0.0 (0 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia