Iklan
Iklan
Pertanyaan
Pada suhu dan tekanan yang sama, lima buah bejana masing-masing berisi lima macam gas dengan data sebagai berikut. Gas dengan massa terbesar terdapat pada bejana ... ( A r C = 12, O = 16, N = 14, H = 1)
Pada suhu dan tekanan yang sama, lima buah bejana masing-masing berisi lima macam gas dengan data sebagai berikut.
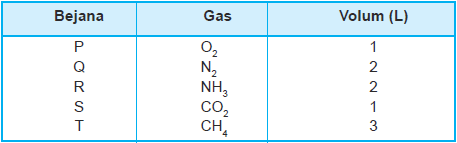
Gas dengan massa terbesar terdapat pada bejana ... ( C = 12, O = 16, N = 14, H = 1)
P
Q
R
S
T
Iklan
AK
A. Kusbardini
Master Teacher
Mahasiswa/Alumni UIN Syarif Hidayatullah Jakarta
Jawaban terverifikasi
8
5.0 (1 rating)
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia














