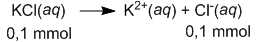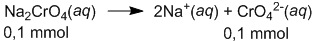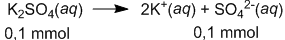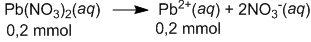Iklan
Iklan
Pertanyaan
Ke dalam 100 mL larutan netral yang merupakan campuran dari garam-garam KCl 1 0 − 3 M, NaCrO 4 1 0 − 3 M,dan K 2 SO 4 1 0 − 3 M ditambahkan 100 mL larutan Pb ( NO 3 ) 2 2 × 1 0 − 3 M. Campuran ini diaduk sampai campur sempurna. Jika Ksp PbCl 2 = 1 , 7 × 1 0 − 5 , PbCrO 4 = 2 × 1 0 − 14 , dan PbSO 4 = 2 × 1 0 − 6 , maka endapan yang terjadi adalah garam ....
Ke dalam 100 mL larutan netral yang merupakan campuran dari garam-garam M, M, dan M ditambahkan 100 mL larutan M. Campuran ini diaduk sampai campur sempurna. Jika Ksp = , = , dan = , maka endapan yang terjadi adalah garam ....
saja
dan
saja
dan
Iklan
IS
I. Solichah
Master Teacher
Jawaban terverifikasi
44
5.0 (1 rating)
OS
Orlyne Syahvira Wijaya
Bantu banget
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia