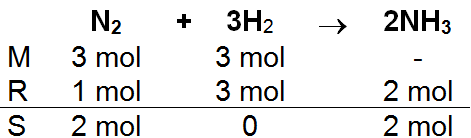Iklan
Iklan
Pertanyaan
Gas nitrogen ( N 2 ) sebanyak 3 mol bereaksi dengan gas hidrogen ( H 2 ) 3 mol. Persamaan reaksi yang terjadi: N 2 ( g ) + H 2 ( g ) → NH 3 ( g ) Tentukan mol gas NH 3 yang terbentuk dan mol zat yang tersisa!
Gas nitrogen sebanyak 3 mol bereaksi dengan gas hidrogen 3 mol. Persamaan reaksi yang terjadi:
Tentukan mol gas yang terbentuk dan mol zat yang tersisa!
Iklan
AK
A. Kusbardini
Master Teacher
Mahasiswa/Alumni UIN Syarif Hidayatullah Jakarta
Jawaban terverifikasi
35
1.0 (2 rating)
AS
Aditya Septian Maulana
Jawaban tidak sesuai
0M
09_I Made Darmayasa
Pembahasan tidak menjawab soal Pembahasan tidak lengkap Jawaban tidak sesuai Pembahasan terpotong
Iklan
Iklan
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2024 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia