IN
Icha N
16 Mei 2022 11:32
Iklan
Iklan
IN
Icha N
16 Mei 2022 11:32
Pertanyaan
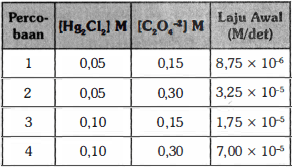
Suatu reaksi dinyatakan dengan persamaan kimia berikut: 2HgCl2 + C2O4^2- → 2Cl^- + 2CO2 + Hg2Cl2 Untuk menentukan laju awal reaksi, pada percobaan dilakukan dengan menggunakan variasi konsentrasi dua pereaksi. Hasilnya diperoleh seperti data pada tabel berikut ini. Persamaan laju untuk reaksi tersebut adalah ... (A) laju = r = k [HgCl2] [C2O4^2-] (B) laju = r = k [HgCl2]^2 [C2O4^2-]^2 (C) laju = r = k [HgCl2] [C2O4^2-]^2 (D) laju = r = k [HgCl2]^2 [C2O4^2-] (E) laju = r = k [HgCl2] [C2O4^2-]^4
3
1
Iklan
Iklan
YA
Y. Ayu
16 Mei 2022 14:23
Jawaban terverifikasi
Jawaban: (C) laju = r = k [HgCl2] [C2O4^2-]^2 Persamaan laju reaksi merupakan sebuah persamaan yang memperlihatkan keterkaitan atau hubungan antara laju reaksi tertentu dengan konsentrasi pereaksinya. Orde reaksi itu merupakan pangkat molaritas dalam persamaan laju reaksi. Orde reaksi diperoleh dari percobaan dengan mencari salah satu orde dari reaktan ketika konsentrasi reaktan lain dibuat tetap. Rumus laju reaksi adalah: r = k [A]^x [B]^y r = laju reaksi (M/s) k = konstanta laju reaksi [A] dan [B]= konsentrasi zat (M) x dan y = orde reaksi Jadi, untuk menentukan persamaan laju reaksinya perlu ditentukan orde reaksi dahulu. Orde reaksi HgCl2 menggunakan data nomor 1 dan 3. r1 = k [HgCl2]^x [C2O4^2-]^y 8,75 x 10^-6 M/s = k (0,05 M)^x (0,15 M)^y r3 = k [HgCl2]^x [C2O4^2-]^y 1,75 x 10^-5 M/s = k (0,1 M)^x (0,15 M)^y Jika kedua persamaan laju dibandingkan, maka didapatkan: r1/r3 = (k [HgCl2]^x [C2O4^2-]^y)/(k [HgCl2]^x [C2O4^2-]^y) (8,75 x 10^-6 M/s)/(1,75 x 10^-5 M/s) = (k (0,05 M)^x (0,15 M)^y)/(k (0,1 M)^x (0,15 M)^y) 1/2 = (0,05 M)^x/(0,1 M)^x x = 1 Orde reaksi C2O4^2- menggunakan data nomor 1 dan 2: r1 = k [HgCl2]^x [C2O4^2-]^y 8,75 x 10^-6 M/s = k (0,05 M)^x (0,15 M)^y r2 = k [HgCl2]^x [C2O4^2-]^y 3,25 x 10^-5 M/s = k (0,05 M)^x (0,3 M)^y Jika kedua persamaan laju dibandingkan, maka didapatkan: r1/r2 = (k [HgCl2]^x [C2O4^2-]^y)/(k [HgCl2]^x [C2O4^2-]^y) (8,75 x 10^-6 M/s)/(3,25 x 10^-5 M/s) = (k (0,05 M)^x (0,15 M)^y)/(k (0,05 M)^x (0,3 M)^y) 1/4 = (0,15 M)^y/(0,3 M)^y 1/4 = (1/2)^y y = 2 Setelah nilai x dan y disubstitusikan, maka persamaan laju reaksinya adalah: r = k [HgCl2] [C2O4^2-]^2 Jadi, persamaan laju reaksi tersebut adalah r = k [HgCl2] [C2O4^2-]^2.
· 0.0 (0)
Iklan
Iklan

Yah, akses pembahasan gratismu habis
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke Forum
Biar Robosquad lain yang jawab soal kamu

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!


