EN
Elisa N
14 Mei 2020 08:34
Iklan
Iklan
EN
Elisa N
14 Mei 2020 08:34
2
1
Iklan
Iklan
IY
I. Yassa
28 Desember 2021 17:13
Jawaban terverifikasi
Haloo kak Elisa ^^ Jawaban dari pertanyaan tersebut adalah pH mula-mula= 3 dan pH setelah ditambahkan H2SO4 adalah 3-log 1,5. Yuk simak pembahasannya agar lebih paham ^^ pH merupakan satuan derajat keasaman pada suatu zat yang memiliki rentang 1-14. Nilai pH diperoleh dari konsentrasi ion H+ pada suatu zat. Pada soal terdapat senyawa HCl yang merupakan asam kuat. Penentuan konsentrasi ion H+ pada asam kuat adalah dengan menggunakan rumus: [H+}= n*Ma dimana: [H+] adalah konsentrasi ion H+ (M), n adalah indeks asam (jumlah atom H pada senyawa asam), dan Ma adalah konsentrasi senyawa asam (M). Perhitungan pH larutan mula-mula dan setelah ditambahkan H2SO4 dijelaskan pada gambar terlampir ^^ semoga membantu~

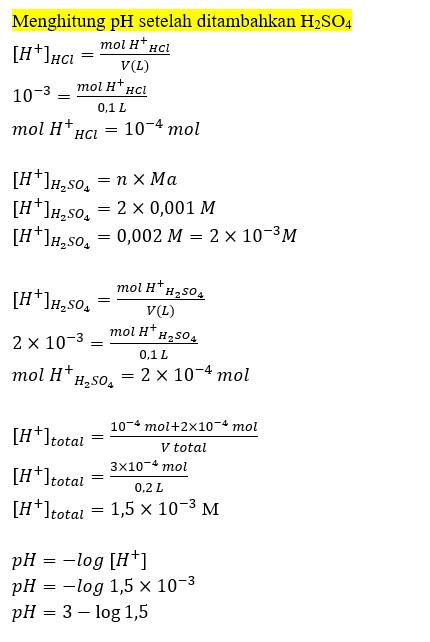
· 0.0 (0)
Iklan
Iklan

Yah, akses pembahasan gratismu habis
Mau pemahaman lebih dalam untuk soal ini?
Tanya ke Forum
Biar Robosquad lain yang jawab soal kamu

LATIHAN SOAL GRATIS!
Drill Soal
Latihan soal sesuai topik yang kamu mau untuk persiapan ujian


Perdalam pemahamanmu bersama Master Teacher
di sesi Live Teaching, GRATIS!


